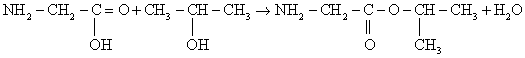Готовимся к ЕГЭ-2018 по химии: разбор демоварианта
Вашему вниманию мы предлагаем разбор демоварианта ЕГЭ 2018 года по химии. В этой статье содержатся пояснения и подробные алгоритмы решения заданий. В помощь при подготовке к ЕГЭ рекомендуем нашу подборку справочников и пособий, а также несколько статей на актуальную тему, опубликованных ранее.Задание 1
Определите, атомы каких из указанных в ряду элементов в основном состоянии имеют на внешнем энергетическом уровне четыре электрона.
1) Na
2) K
3) Si
4) Mg
5)
C
Ответ: Периодическая система химических элементов – графическое отображение Периодического закона. Она состоит из периодов и групп. Группа – это вертикальный столбец химических элементов, состоит из главной и побочной подгрупп. Если элемент находится в главной подгруппе определенной группы, то номер группы говорит о количестве электронов на последнем слое. Следовательно, чтобы ответить на данный вопрос необходимо открыть таблицу Менделеева и посмотреть, какие элементы из представленных в задании расположены в одной группе. Приходим к выводу, что такими элементами являются: Si и C, следовательно ответ будет: 3; 5.
Задание 2
Из указанных в ряду химических элементов
1) Na
2) K
3) Si
4) Mg
5) C
выберите три элемента, которые в Периодической системе химических элементов Д.И.Менделеева находятся в одном периоде.
Расположите химические элементы в порядке возрастания их металлических свойств.
Запишите в поле ответа номера выбранных химических элементов в нужной последовательности.
Ответ: Периодическая система химических элементов – графическое отображение Периодического закона. Она состоит из периодов и групп. Период – это горизонтальный ряд химических элементов, расположенных в порядке возрастания электроотрицательности, а значит, уменьшения металлических свойств и усиления неметаллических. Каждый период (за исключением первого) начинается с активного металла, который называется щелочным, и заканчивается инертным элементом, т.е. элементом, который не образует химических соединений с другими элементами (за редким исключением).
Глядя на таблицу химических элементов, отмечаем, что из данных в задании элементов, Na, Mg и Si расположены в 3 периоде. Далее необходимо расположить эти элементы в порядке возрастания металлических свойств. Из написанного выше определяем, если металлические свойства убывают слева на право, значит возрастают они наоборот, справа налево. Поэтому правильными ответами будут 3; 4; 1.

Задание 3
Из числа указанных в ряду элементов
1) Na
2) K
3) Si
4) Mg
5) C
выберите два элемента, которые проявляют низшую степень окисления –4.
Ответ: Высшая степень окисления химического элемента в соединении численно равна номеру группы, в которой находится химический элемент со знаком плюс. Если элемент расположен в 1 группе, то его высшая степень окисления равна +1, во второй группе +2 и так далее. Низшая степень окисления химического элемента в соединениях равна 8 (высшая степень окисления, которую может проявить химический элемент в соединении) минус номер группы, со знаком минус. Например, элемент стоит в 5 группе, главной подгруппе; следовательно, высшая степень окисления его в соединениях будет равна +5; низшая степень окисления соответственно 8 – 5 = 3 со знаком минус т.е. –3. У элементов 4 периода высшая валентность равна +4, а низшая –4. Поэтому ищем из списка элементов данных в задании два элемента расположенных в 4 группе главной подгруппе. Это будет C и Si номера правильного ответа 3; 5.
Задание 4
Из предложенного перечня выберите два соединения, в которых присутствует ионная связь.
1) Ca(ClO2)2
2) HClO3
3) NH4Cl
4) HClO4
5) Cl2O7
Ответ: Под химической связью понимают такое взаимодействие атомов, которое связывает их в молекулы, ионы, радикалы, кристаллы. Различают четыре типа химических связей: ионную, ковалентную, металлическую и водородную.
Ионная связь –
связь, возникающая в результате электростатического притяжения разноименно
заряженных ионов (катионов и анионов), иными словами, между типичным
металлом и типичным неметаллом; т.е. элементами, резко отличающимися
друг от друга по электроотрицательности. ( > 1,7
по шкале Полинга). Ионная связь присутствует в соединениях, содержащих
металлы 1 и 2 групп главных подгрупп (за исключением Mg и Be)
и типичных неметаллов; кислорода и элементов 7 группы главной
подгруппы. Исключение составляют соли аммония, они не содержат атома
металла, вместо него ион 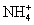 , но в солях
аммония между ионом аммония и кислотного остатка – связь тоже ионная.
Поэтому правильными ответами будут 1; 3.
, но в солях
аммония между ионом аммония и кислотного остатка – связь тоже ионная.
Поэтому правильными ответами будут 1; 3.
Задание 5
Установите соответствие между формулой вещества и классов / группой, к которому(-ой) это вещество принадлежит: к каждой позиции, обозначенной буквой, подберите соответствующую позицию, обозначенную цифрой.
|
ФОРМУЛА ВЕЩЕСТВА |
КЛАСС / ГРУППА |
|
А) NH4HCO3 |
1) соли средние |
|
Б) KF |
2) оксиды кислотные |
|
В) NO |
3) оксиды несолеобразующие |
|
|
4) соли кислые |
Запишите в таблицу выбранные цифры под соответствующими буквами.
| Ответ: | А |
Б |
В |
|
|
|
|
|
Ответ: Для ответа на данный вопрос мы должны вспомнить, что такое оксиды и соли. Соли – это сложные вещества, состоящие из ионов металла и ионов кислотного остатка. Исключение составляют соли аммония. У данных солей вместо ионов металла стоит ион аммония. Соли бывают средними, кислыми, двойными, основными и комплексными. Средние соли – это продукты полного замещения водорода кислоты на металл или ион аммония; например:
H2SO4 + 2Na = H2 + Na2SO4.
Данная соль является средней. Кислые соли – это продукт неполного замещения водорода соли на металл; например:
2H2SO4 + 2Na = H2 + 2NaHSO4.
Данная соль является кислой. Теперь давайте посмотрим на наше задание. В нем содержится две соли: NH4HCO3 и KF. Первая соль является кислой, поскольку это продукт неполного замещения водорода в кислоте. Поэтому в табличке с ответом под буквой «А» поставим цифру 4; другая соль (KF) не содержит водорода между металлом и кислотным остатком, поэтому в табличке с ответом под буквой «Б» поставим цифру 1. Оксиды – это бинарное соединение, в состав которого входит кислород. Он стоит на втором месте и проявляет степень окисления –2. Оксиды бывают основными (т.е. оксиды металлов, например Na2O, CaO – им соответствуют основания; NaOH и Ca(OH)2 ), кислотными (т.е. оксиды неметаллов P2O5, SO3 – им соответствуют кислоты; H3PO4 и H2SO4), амфотерными (оксиды, которые в зависимости от обстоятельств могут проявлять основные и кислотные свойства – Al2O3, ZnO) и несолеобразующие. Это оксиды неметаллов, которые не проявляют ни основных, ни кислотных, ни амфотерных свойств; это CO, N2O, NO. Следовательно, оксид NO является несолеобразующим оксидом, поэтому в табличке с ответом под буквой «В» поставим цифру 3. И заполненная таблица будет иметь следующий вид:
| Ответ: | А |
Б |
В |
|
4 |
1 |
3 |

Задание 6
Из предложенного перечня выберите два вещества, с каждым из которых железо реагирует без нагревания.
1) хлорид
кальция (р-р)
2) сульфат меди
(II) (р-р)
3) концентрированная
азотная кислота
4) разбавленная
соляная кислота
5) оксид алюминия
Ответ: Железо – активный металл. Взаимодействует с хлором, углеродом и другими неметаллами при нагревании:
2Fe + 3Cl2 = 2FeCl3
Вытесняет из растворов солей металлы, находящиеся в электрохимическом ряду напряжений правее железа:
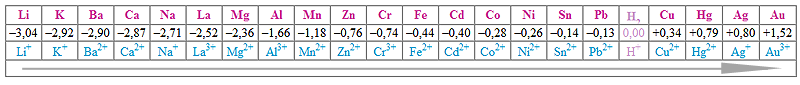 Например:
Например:
Fe + CuSO4 = FeSO4 + Cu
Растворяется в разбавленных серной и соляной кислотах c выделением водорода,
Fe + 2НCl = FeCl2 + H2
с раствором азотной кислоты
Fe + 4HNO3 = Fe(NO3)3 + NO + 2H2O.
Концентрированные серная и соляная кислота при обычных условиях с железом не реагируют, они его пассивируют:
Исходя из этого правильными ответами будут: 2; 4.
Задание 7
В одну из пробирок с осадком гидроксида алюминия добавили сильную кислоту Х, а в другую – раствор вещества Y. в результате в каждой из пробирок наблюдали растворение осадка. Из предложенного перечня выберите вещества Х и Y, которые могут вступать в описанные реакции.
1)
бромоводородная кислота.
2)
гидросульфид натрия.
3)
сероводородная кислота.
4)
гидроксид калия.
5)
гидрат аммиака.
Запишите
в таблицу номера выбранных веществ под соответствующими буквами.
Ответ: Гидроксид алюминия является амфотерным основанием, поэтому может взаимодействовать с растворами кислот и щелочей:
1) Взаимодействие с раствором кислоты: Al(OH)3 + 3HBr = AlCl3 + 3H2O.
При этом осадок гидроксида алюминия растворяется.
2) Взаимодействие со щелочами: 2Al(OH)3 + Сa(OH)2 = Ca[Al(OH)4]2.
При этом осадок гидроксида алюминия также растворяется.
| Ответ: | X |
Y |
|
|
1 |
4 |
|
Задание 8
Установите соответствие между формулой вещества и реагентами, с каждым из которых это вещество может взаимодействовать: к каждой позиции, обозначенной буквой, подберите соответствующую позицию, обозначенную цифрой
|
ФОРМУЛА ВЕЩЕСТВА |
РЕАГЕНТЫ |
А) S Б) SO3 В) Zn(OH)2 Г) ZnBr2 (р-р) |
1) AgNO3, Na3PO4, Cl2 2) BaO, H2O, KOH 3) H2, Cl2, O2 4) НBr, LiOH, CH3COOH (р-р) 5) H3PO4 (р-р), BaCl2, CuO |
Ответ: Под буквой А стоит сера (S). Как простое вещество, сера может вступать в окислительно-восстановительные реакции. Большинство реакций происходит с простыми веществами, металлами и неметаллами. Окисляется растворами концентрированных серной и соляной кислот. Взаимодействует со щелочами. Из всех реагентов, расположенных под цифрами 1–5, больше всего под описанные выше свойства подходят простые вещества под цифрой 3.
S + H2 = H2S
S + Cl2 = SCl2
S + O2 + SO2
Следующее вещество – SO3, буква Б. Оксид серы VI – сложное вещество, кислотные оксид. Данный оксид содержит серу в степени окисления +6. Это высшая степень окисления серы. Поэтому SO3 будет вступать в реакции, в качестве окислителя, с простыми веществами, например с фосфором, со сложными веществами, например с KI, H2S. При этом его степень окисления может понизиться до +4, 0 или –2, также вступает в реакции без изменения степени окисления с водой, оксидами металлов и гидроксидами. Исходя из этого, SO3 будет реагировать со всеми реагентами под цифрой 2, то есть:
SO3 + BaO = BaSO4
SO3 + H2O = H2SO4
SO3 + 2KOH = K2SO4 + H2O
Zn(OH)2 – амфотерный гидроксид расположен под буквой В. Обладает уникальными свойствами – реагирует как с кислотами, так и со щелочами. Поэтому из всех представленных реагентов можно смело выбирать реагенты под цифрой 4.
Zn(OH)2 + HBr = ZnBr2 + H2O
Zn(OH)2 + LiOH = Li2[Zn(OH)4]
Zn(OH)2 + CH3COOH = (CH3COO)2Zn + H2O
И наконец, под буквой Г расположено вещество ZnBr2 – соль, бромид цинка. Соли реагируют с кислотами, щелочами, другими солями, а также соли бескислородных кислот, как и данная соль, могут взаимодействовать с неметаллами. В данном случае наиболее активные галогены (Cl или F) могут вытеснять менее активные (Br и I) из растворов их солей. Данным критериям соответствуют реагенты под цифрой 1.
ZnBr2 + 2AgNO3 = 2AgBr + Zn(NO3)2
3ZnBr2 + 2Na3PO4 = Zn3(PO4)2 + 6NaBr
ZnBr2 + Cl2 = ZnCl2 + Br2
Варианты ответа выглядят следующим образом:
|
А |
Б |
В |
Г |
|
3 |
2 |
4 |
1 |

Задание 9
Установите соответствие между исходными веществами, вступающими в реакцию, и продуктами этой реакции: к каждой позиции, обозначенной буквой, подберите соответствующую позицию, обозначенную цифрой.
|
ИСХОДНЫЕ ВЕЩЕСТВА |
ПРОДУКТЫ РЕАКЦИИ |
А) Mg и H2SO4 (конц) Б) MgO и H2SO4 В) S и H2SO4 (конц) Г) H2S и O2 (изб.) |
1) MgSO4 и H2O 2) MgO, SO2, и H2O 3) H2S и H2O 4) SO2 и H2O 5) MgSO4, H2S и H2O 6) SO3 и H2O |
Ответ: А) Серная кислота концентрированная является сильным окислителем. Может взаимодействовать и с металлами стоящими в электрохимическом ряду напряжений металлов после водорода. При этом водород, как правило, в свободном состоянии не выделяется, он окисляется в воду, а серная кислота восстанавливается до различных соединений, например: SO2, S и H2S, в зависимости от активности металла. При взаимодействии с магнием реакция будет иметь следующий вид:
4Mg + 5H2SO4 (конц) = 4MgSO4 + H2S + H2O (цифра ответа 5)
Б) При взаимодействии серной кислоты с оксидом магния образуются соль и вода:
MgO + H2SO4 = MgSO4 + H2O (Цифра ответа 1)
В) Концентрированная серная кислота окисляет не только металлы, но и неметаллы, в данном случае серу, по следующему уравнению реакции:
S + 2H2SO4 (конц) = 3SO2 + 2H2O (цифра ответа 4)
Г) При горении сложных веществ с участием кислорода образуются оксиды всех элементов, входящих в состав сложного вещества; например:
2H2S + 3O2 = 2SO2 + 2H2O (цифра ответа 4)
Таким образом, общий ответ будет иметь следующий вид:
А |
Б |
В |
Г |
5 |
1 |
4 |
4 |
Задание 10
Задана следующая схема превращений веществ:
| Х | Y | |||
| K2CO3 | → | CO2 | → | KHCO3 |
Определите, какие из указанных веществ являются веществами X и Y.
1) KCl (р-р)
2) KOH (р-р)
3) H2
4) HCl (избыток)
5) CO2
Ответ: Карбонаты вступают в химическую реакцию с кислотами, при этом образуется слабая угольная кислота, которая в момент образования разлагается на углекислый газ и воду:
K2CO3 + 2HCl(избыток) = 2KCl + CO2 + H2O
При пропускании через раствор гидроксида калия избытка углекислого газа образуется гидрокарбонат калия.
CO2 + КОН = KHCO3
Записываем в таблицу ответ:
X |
Y |
4 |
2 |
Задание 11
Установите соответствие между названием вещества и классом/группой, к которому(-ой) это вещество принадлежит: к каждой позиции, обозначенной буквой, подберите соответствующую позицию, обозначенную цифрой.
|
НАЗВАНИЕ ВЕЩЕСТВА |
КЛАСС/ГРУППА |
А) метилбензол Б) анилин В) 3-метилбутаналь |
1) альдегиды 2) амины 3) аминокислоты 4) углеводороды |
Ответ: А) Метилбензол относится к гомологическому ряду ароматических углеводородов; его формула C6H5CH3 (цифра 4)
Б) Анилин относится к гомологическому ряду ароматических аминов. Его формула C6H5NH2. Группа NH2 – функциональная группа аминов. (цифра 2)
В) 3-метилбутаналь относится к гомологическому ряду альдегидов. Так как альдегиды имеют окончание -аль. Его формула:
| CH3– | CH– | CH2–COH |
| │ | ||
| CH3 |
|
Записываем в таблицу ответ:
|
А |
Б |
В |
|
4 |
2 |
1 |

Задание 12
Из предложенного перечня выберите два вещества, которые являются структурными изомерами бутена-1.
1) бутан
2) циклобутан
3) бутин-2
4) бутадиен-1,3
5) метилпропен
Ответ: Изомеры – это вещества, имеющие одинаковую молекулярную формулу, но различные строение и свойства. Структурные изомеры – это тип веществ, которые идентичны друг другу по количественному и качественному составам, но порядок атомного связывания (химического строения) имеет различия. Для ответа на этот вопрос давайте напишем молекулярные формулы всех веществ. Формула бутена-1 будет выглядеть так: С4Н8
1) бутан – С4Н10
2) циклобутан –
С4Н8
3) бутин-2 – С4Н6
4) бутадиен-1, 3
– С4Н6
5) метилпропен –
С4Н8
Такие же формулы имеют циклобутан № 2 и метилпропен № 5. Они и будут структурными изомерами бутена-1.
Записываем в таблицу правильные ответы:
|
2 |
5 |
Задание 13
Из предложенного перечня выберите два вещества, при взаимодействии которых с раствором перманганата калия в присутствии серной кислоты будет наблюдаться изменение окраски раствора.
1) гексан
2) бензол
3) толуол
4) пропан
5) пропилен
Ответ: Давайте попробуем ответить на этот вопрос методом исключения. Предельные углеводороды не подвергаются окислению данным окислителем, поэтому вычеркиваем гексан № 1 и пропан № 4.
Далее – бензольное кольцо устойчиво к действию подавляющего большинства окислителей.
Вычеркиваем № 2 (бензол). У гомологов бензола алкильные группы легко окисляются под действием таких окислительных агентов, как перманганат калия. Поэтому толуол (метилбензол) будет подвергаться окислению по метильному радикалу. Так же окисляется и пропилен (непредельный углеводород с двойной связью).
Правильный ответ:
|
3 |
5 |
Задание 14
Из предложенного перечня выберите два вещества, с которыми реагирует формальдегид.
1) Cu
2) N2
3) H2
4) Ag2O (NH3 р-р)
5) CH3OCH3
Ответ: Формальдегид – это альдегид муравьиной кислоты. Он вступает во многие химические реакции, но основными являются реакции восстановления и окисления. Восстановителем может служить водород, который присоединяется по связи: С=О, превращая его в метанол
| Н– | С | =О + Н2 = СН3ОН |
| │ | ||
| Н |
Окисляются альдегиды различными окислителями, в том числе и аммиачным раствором оксида серебра (знаменитая реакция серебряного зеркала)
| Н– | С | =О + Ag2O (NH3 р-р) =H– | C | =O + 2Ag |
| │ | │ | |||
| Н | О | Н |
Правильный ответ:
|
3 |
4 |

Задание 15
Из предложенного перечня выберите два вещества, с которыми реагирует метиламин.
1) пропан
2) хлорметан
3) водород
4) гидроксид
натрия
5) соляная
кислота.
Ответ: Амины, являясь производными аммиака, имеют сходное с ним строение и проявляют подобные ему свойства. Для них также характерно образование донорно-акцепторной связи. Как и аммиак, они вступают в реакцию с кислотами. Например, с соляной кислотой с образованием хлорида метиламмония.
CH3–NH2 + HCl =[CH3NH3]Cl.
Из органических веществ метиламин вступает в реакции алкилирования с галогеналканами:
CH3–NH2 + CH3Cl = [(CH3)2NH2]Cl
С другими веществами из данного списка амины не реагируют, поэтому правильный ответ:
|
2 |
5 |
Задание 16
Установите соответствие между названием вещества и продуктом, который преимущественно образуется при взаимодействии этого вещества с бромом: к каждой позиции, обозначенной буквой, выберите соответствующую позицию, обозначенную цифрой.
НАЗВАНИЕ ВЕЩЕСТВА |
ПРОДУКТЫ БРОМИРОВАНИЯ |
||||||||||||||||||||||||
А) этан Б) изобутан В) циклопропан Г) циклогексан |
1)
3) Br–CH2–CH2–CH2–Br
5) CH3–CH2–Br 6) |
Ответ: А) этан – это предельный углеводород. Для него не характерны реакции присоединения, поэтому происходит замещение атома водорода на бром. И получается бромэтан:
CH3–СH3 + Br2 = CH3–CH2–Br + HBr (ответ 5)
Б) Изобутан, так же как и этан, – представитель предельных углеводородов, поэтому для него характерны реакции замещения водорода на бром. В отличие от этана, изобутан содержит не только первичные атомы углерода (соединенные с тремя атомами водорода), но и один первичный атом углерода. А так как замещение атома водорода галогеном легче всего идет у менее гидрогенизированного третичного атома углерода, затем у вторичного и в последнюю очередь у первичного, бром будет присоединяться именно к нему. В результате получим 2-бром, 2-метилпропан:
| C | H3 | C | H3 | ||
| │ | │ | ||||
| CH3– | C | –CH3 + Br2 = CH3– | C | –CH3 + HBr | (ответ 2) |
| │ | │ | ||||
| Н | B | r |
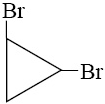
В) Циклоалканы, к которым относится циклопропан, сильно отличаются между собой по устойчивости цикла: наименее устойчивы трехчленные и наиболее устойчивы пяти- и шестичленные циклы. При бромировании 3-х и 4-х членных циклов, происходит их разрыв с образованием алканов. При этом присоединяются сразу 2 атома брома.
|
|
+ Br2 = Br–CH2–CH2–CH2–Br (ответ 3) |
Г) Реакция взаимодействия с бромом у пяти и шестичленных циклов не приводит к разрыву цикла, а сводится к реакции замещения водорода на бром.
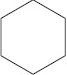 |
+ Br2 = |
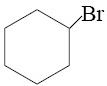 |
+ HBr (ответ 6) |
Таким образом, общий ответ будет иметь вид:
|
А |
Б |
В |
Г |
|
5 |
2 |
3 |
6 |
Задание 17
Установите соответствие между реагирующими веществами и углеродсодержащим продуктом, который образуется при взаимодействии этих веществ: к каждой позиции, обозначенной буквой, подберите соответствующую позицию, обозначенную цифрой.
|
РЕАГИРУЮЩИЕ ВЕЩЕСТВА |
ПРОДУКТ ВЗАИМОДЕЙСТВИЯ |
А) уксусная кислота и сульфид натрия Б) муравьиная кислота и гидроксид натрия В) муравьиная кислота и гидроксид меди (II) (при нагревании) Г) этанол и натрий |
1) пропионат натрия 2) этилат натрия 3) формиат меди (II) 4) формиат натрия 5) ацетат натрия 6) углекислый газ |
Ответ: А) Реакция между уксусной кислотой и сульфидом натрия относится к реакциям обмена, когда сложные вещества обмениваются составными частями.
CH3COOH + Na2S = CH3COONa + H2S.
Cоли уксусной кислоты называются ацетаты. Данная соль, соответственно, называется ацетат натрия. Ответ под цифрой 5
Б) Реакция между муравьиной кислотой и гидроксидом натрия также относится к реакциям обмена.
HCOOH + NaOH = HCOONa + H2O.
Соли муравьиной кислоты называются формиаты. В данном случае образуется формиат натрия. Ответ под цифрой 4.
В) Муравьиная кислота, в отличие от других карбоновых кислот – удивительное вещество. Содержит в себе помимо функциональной карбоксильной группы –СООН, еще и альдегидную группу СОН. Поэтому они вступают в реакции характерные для альдегидов. Например, в реакцию серебряного зеркала; восстановления гидроксида меди (II), Cu(OH)2 при нагревании до гидроксида меди (I), CuOH, разлагающегося при высокой температуре до оксида меди (I), Cu2O. Образуется красивый осадок оранжевого цвета.
2Cu(OH)2 + 2HCOOH = 2СO2 + 3H2O + Cu2O
Сама же муравьиная кислота окисляется до углекислого газа. (правильный ответ 6)
Г) При взаимодействии этанола с натрием образуется газообразный водород и этилат натрия.
2C2H5OH + 2Na = 2C2H5ONa + H2 (ответ 2)
Таким образом, на данное задание ответами будут:
|
А |
Б |
В |
Г |
|
5 |
4 |
6 |
2 |

Задание 18
Задана следующая схема превращения веществ:
| Х | Y | |||
| CH3CH2Cl | → | CH3CH2OH | → | CH3CHO |
Определите, какие из указанных веществ являются веществами X и Y.
1) H2
2) CuO
3) Cu(OH)2
4) NaOH (H2O)
5) NaOH (спирт)
Ответ: Галогеноводороды обладают способностью подвергаться гидролизу. В данном случае при взаимодействии хлорэтана с раствором гидроксида натрия приведет к щелочному гидролизу.
| H2O | ||
| CH3CH2Cl + NaOH | → | CH3CH2OH + NaCl (ответ 4) |
Спирты при высокой температуре в присутствии окислителей могут окисляться до соответствующих альдегидов. В данном случае в качестве окислителя служит оксид меди II (CuO) по следующей реакции:
СH3CH2OH + CuO (t) = СH3COH + Cu + H2O (ответ: 2)
Общий ответ данного номера:
|
X |
Y |
|
4 |
2 |
Задание 19
Из предложенного перечня типов реакций выберите два типа реакции, к которым можно отнести взаимодействие щелочных металлов с водой.
1)
каталитическая
2) гомогенная
3) необратимая
4)
окислительно-восстановительная
5) реакция нейтрализации
Ответ: Напишем уравнение реакции, например, натрия с водой:
2Na +2H2O = 2NaOH + H2.
Натрий, очень активный металл, поэтому с водой будет энергично взаимодействовать, в некоторых случаях даже со взрывом, поэтому реакция идет без катализаторов. Натрий – это металл, твердое вещество, вода и раствор гидроксида натрия – жидкости, водород – газ, поэтому реакция гетерогенная. Реакция необратимая, потому что водород уходит из реакционной среды в виде газа. В процессе реакции изменяются степени окисления у натрия и водорода,
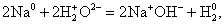
поэтому реакция относится к окислительно-восстановительным, так как натрий выступает в роли восстановителя, а водород в роли окислителя. К реакциям нейтрализации не относится, поскольку в результате реакции нейтрализации образуются вещества, имеющие нейтральную реакцию среды, а здесь образуется щелочь. Из этого можно сделать вывод, что правильными будут ответы
|
3 |
4 |
Задание 20
Из предложенного перечня внешних воздействий выберите два воздействия, которые приводят к уменьшению скорости химической реакции этилена с водородом:
1) понижение
температуры
2) увеличение
концентрации этилена
3) использование
катализатора
4) уменьшение
концентрации водорода
5) повышение
давления в системе.
Ответ: Скорость химической реакции – это величина, показывающая, как изменяются концентрации исходных веществ или продуктов реакции за единицу времени. Существует понятие скорости гомогенных и гетерогенных реакций. В данном случае дана гомогенная реакция, поэтому для гомогенных реакций скорость зависит от следующих взаимодействий (факторов):
- концентрация реагирующих веществ;
- температура;
- катализатор;
- ингибитор.
Данная реакция проходит при повышенной температуре, поэтому понижение температуры приведет к уменьшению ее скорости. Ответ № 1. Далее: если увеличить концентрацию одного из реагирующих веществ, реакция пойдет быстрее. Нам это не подходит. Катализатор – вещество, увеличивающее скорость реакции, – тоже не подходит. Уменьшение концентрации водорода приведет к замедлению реакции, что нам и нужно. Значит, еще один правильный ответ – № 4. Для ответа на пункт 4 вопроса давайте напишем уравнение данной реакции:
CH2=CH2 + H2 = CH3-CH3.
Из уравнения реакции видно, что она идет с уменьшением объема (в реакцию вступило 2 объема веществ – этилен + водород), а образовался только один объем продукта реакции. Следовательно, при увеличении давления скорость реакции должна увеличиться – тоже не подходит. Подведем итог. Правильными оказались ответы:
|
1 |
4 |

Задание 21
Установите соответствие между уравнением реакции и свойством элемента азота, которое он проявляет в этой реакции: к каждой позиции, обозначенной буквой, подберите соответствующую позицию, обозначенную цифрой.
|
УРАВНЕНИЕ РЕАКЦИИ |
СВОЙСТВА АЗОТА |
А) NH4HCO3 = NH3 + H2O + CO2 Б) 3CuO + 2NH3 = N2 + 3Cu + 3H2O В) 4NH3 + 5O2 = 4NO + 6H2O |
1) является окислителем 2) является восстановителем 3) является и окислителем, и восстановителем 4) не проявляет окислительно-восстановительных свойств |
Ответ: Посмотрим, как изменяются степени окисления в реакциях:
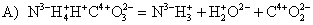
в данной реакции азот не изменяет степени окисления. Она у него в реакции стабильна 3–. Поэтому ответ 4.

в данной реакции азот изменяет свою степень окисления с 3– до 0, то есть окисляется. Значит, он является восстановителем. Ответ 2.
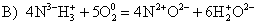
Здесь азот изменяет свою степень окисления с 3– до 2+. Реакция окислительно-восстановительная, азот окисляется, значит, является восстановителем. Правильный ответ 2.
Общий ответ:
|
А |
Б |
В |
|
4 |
2 |
2 |
Задание 22
Установите соответствие между формулой соли и продуктами электролиза водного раствора этой соли, которые выделились на инертных электродах: к каждой позиции, обозначенной буквой, подберите соответствующую позицию, обозначенную цифрой.
|
ФОРМУЛА СОЛИ |
ПРОДУКТЫ ЭЛЕКТРОЛИЗА |
А) Na3PO4 Б) KCl В) CuBr2 Г) Cu(NO3)2 |
1) H2, O2 2) Cu, O2 3) Cu, Br2 4) H2, Cl2 5) Cu, NO2 |
Ответ: Электролиз – это окислительно-восстановительная реакция, протекающая на электродах, при прохождении постоянного электрического тока через раствор или расплав электролита. На катоде всегда идёт процесс восстановления; на аноде всегда идёт процесс окисления. Если металл стоит в электрохимическом ряду напряжений металлов до марганца, то на катоде восстанавливается вода; от марганца до водорода возможно выделение воды и металла, если правее водорода, то восстанавливается только металл. Процессы, протекающие на аноде:
Если анод инертный, то в случае бескислородных анионов (кроме фторидов) идет окисление анионов:

В случае кислородсодержащих анионов и фторидов идет процесс окисления воды, анион при этом не окисляется и остается в растворе:

При электролизе растворов щелочей идет окисление гидроксид-ионов:

Теперь давайте рассмотрим данное задание:
А) Na3PO4 диссоциирует в растворе на ионы натрия и кислотного остатка кислородсодержащей кислоты.

Катион натрия устремляется к отрицательному электроду – катоду. Так как ион натрия в электрохимическом ряду напряжений металлов находится до алюминия, то от восстанавливаться не будет, будет восстанавливаться вода по следующему уравнению:
2H2O = H2 + 2OH–.
На катоде выделяется водород.
Анион
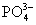 устремляется к аноду – положительно
заряженному электроду – и находится в прианодном пространстве,
а на аноде окисляется вода по уравнению:
устремляется к аноду – положительно
заряженному электроду – и находится в прианодном пространстве,
а на аноде окисляется вода по уравнению:
2H2O – 4e = O2↑ + 4H+
На аноде происходит выделение кислорода. Таким образом, суммарное уравнение реакции будет иметь следующий вид:
2Na3PO4 + 8H2O = 2H2 + O2 + 6NaOH + 2 H3PO4 (ответ 1)
Б) при электролизе раствора КCl на катоде будет восстанавливаться вода по уравнению:
2H2O = H2 + 2OH–.
В качестве продукта реакции будет выделяться водород. На аноде будет окисляться Cl– до свободного состояния по следующему уравнению:
2CI– – 2e = Cl2.
Суммарный процесс на электродах выглядит следующим образом:
2KCl + 2H2O = 2KOH + H2 + Cl2 (ответ 4)
В) При электролизе соли CuBr2 на катоде восстанавливается медь:
Cu2+ + 2e = Cu0.
На аноде окисляется бром:

Суммарное уравнение реакции будет иметь следующий вид:

Правильный ответ 3.
Г) Гидролиз соли Cu(NO3)2 протекает следующим образом: на катоде происходит выделение меди по следующему уравнению:
Cu2+ + 2e = Cu0.
На аноде выделяется кислород:
2H2O – 4e = O2↑ + 4H+
Правильный ответ 2.
Общий ответ на данный вопрос:
|
А |
Б |
В |
Г |
|
1 |
4 |
3 |
2 |

Задание 23
Установите соответствие между названием соли и отношением этой соли к гидролизу: к каждой позиции, обозначенной буквой, подберите соответствующую позицию, обозначенную цифрой.
|
НАЗВАНИЕ СОЛИ |
ОТНОШЕНИЕ К ГИДРОЛИЗУ |
А) хлорид аммония Б) сульфат калия В) карбонат натрия Г) сульфид алюминия |
1) гидролизуется по катиону 2) гидролизуется по аниону 3) гидролизу не подвергается 4) гидролизуется по катиону и аниону |
Ответ: Гидролизом называется реакция взаимодействия ионов соли с молекулами воды, приводящая к образованию слабого электролита. Любую соль можно представить как продукт взаимодействия кислоты и основания. По этому принципу все соли можно разделить на 4 группы:
- Соли, образованные сильным основанием и слабой кислотой.
- Соли, образованные слабым основанием и сильной кислотой.
- Соли, образованные слабым основанием и слабой кислотой.
- Соли, образованные сильным основанием и сильной кислотой.
Давайте теперь разберем с этой точки зрения данное задание.
А) NH4Cl – соль, образованная слабым основанием NH4OH и сильной кислотой HCl – подвергается гидролизу. В результате
образуется слабое основание и сильная кислота. Данная соль гидролизуется
по катиону 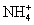 , так как данный ион входит в состав
слабого основания. Ответ под цифрой 1.
, так как данный ион входит в состав
слабого основания. Ответ под цифрой 1.
Б) K2SO4 – соль, образованная сильным основанием и сильной кислотой. Такие соли гидролизу не подвергаются, так как не образуется слабого электролита. Ответ 3.
В) Карбонат натрия Na2CO3 – соль, образованная сильным основанием NaOH и слабой угольной кислотой H2CO3 – подвергается гидролизу. Так как соль образована двухосновной кислотой, то гидролиз теоретически может идти в две стадии. в результате первой стадии образуется щелочь и кислая соль – гидрокарбонат натрия:
Na2CO3 + H2O ↔NaHCO3 + NaOH;
в результате второй стадии образуется слабая угольная кислота:
NaHCO3 + H2O ↔ H2CO3 (H2O + CO2) + NaOH –
данная соль гидролизуется по аниону  (ответ 2).
(ответ 2).
Г) Соль сульфид алюминия Al2S3 образована слабым основанием Al(OH)3 и слабой кислотой H2S. Такие соли подвергаются гидролизу. В результате образуется слабое основание и слабая кислота. Гидролиз идет по катиону и аниону. Правильный ответ 4.
Таким образом, общий ответ на задание имеет вид:
|
А |
Б |
В |
Г |
|
1 |
3 |
2 |
4 |
Задание 24
Установите соответствие между уравнением обратимой реакции и направлением смещения химического равновесия при увеличении давления: к каждой позиции, обозначенной буквой, подберите соответствующую позицию, обозначенную цифрой.
|
УРАВНЕНИЕ РЕАКЦИИ |
НАПРАВЛЕНИЕ СМЕЩЕНИЯ ХИМИЧЕСКОГО РАВНОВЕСИЯ |
А) N2(г) + 3H2(г) = 2NH3(г) Б) 2H2(г) + O2(г) = 2H2O(г) В) H2(г) + CI2(г) = 2HCl(г) Г) SO2(г) + CI2(г) = SO2Cl2(г) |
1) смещается в сторону прямой реакции 2) смещается в сторону обратной реакции 3) практически не смещается. |
Ответ: Обратимыми называют реакции, которые одновременно могут идти в двух противоположных направлениях: в сторону прямой и обратной реакции, поэтому в уравнениях обратимых реакций вместо равенства ставится знак обратимости. Каждая обратимая реакция заканчивается химическим равновесием. Это динамический процесс. Для того чтобы вывести реакцию из состояния химического равновесия, нужно приложить к ней определенные внешние воздействия: изменить концентрацию, температуру или давление. Делается это по принципу Ле-Шателье: если на систему, находящуюся в состоянии химического равновесия, подействовать извне, изменить концентрацию, температуру или давление, то система стремится занять такое положение, которое противодействует этому действию.
Разберем это на примерах нашего задания.
А) Гомогенная реакция N2(г) + 3H2(г) = 2NH3(г) является еще и экзотермической, то есть идет с выделением теплоты. Далее в реакцию вступило 4 объема реагирующих веществ (1 объем азота и 3 объема водорода), а в результате образовался один объем аммиака. Таким образом, мы определили, что реакция идет с уменьшением объема. По принципу Ле-Шателье, если реакция идет с уменьшением объема, то увеличение давления смещает химическое равновесие в сторону образования продукта реакции. Правильный ответ 1.
Б) Реакция 2H2(г) + O2(г) = 2H2O(г) аналогична предыдущей реакции, также идет с уменьшением объема (вступило 3 объема газа, а в результате реакции образовалось 2), поэтому увеличение давления сместит равновесие в сторону образования продукта реакции. Ответ 1.
В) Данная реакция H2(г) + Cl2(г) = 2HCl(г) протекает без изменения объема реагирующих веществ (вступило 2 объема газов и образовалось 2 объема хлороводорода). На реакции, идущие без изменения объема, давление влияния не оказывает. Ответ 3.
Г) Реакция взаимодействия оксида серы (IV) и хлора SO2(г) + Cl2(г) = SO2Cl2(г) является реакцией, идущей с уменьшением объема веществ (в реакцию вступило 2 объема газов, а образовался один объем SO2Cl2). Ответ 1.
Ответом на это задание будет следующий набор букв и цифр:
|
А |
Б |
В |
Г |
|
1 |
1 |
3 |
1 |

Задание 25
Установите соответствие между формулами веществ и реагентом, с помощью которого можно различить водные растворы этих веществ: к каждой позиции, обозначенной буквой, подберите соответствующую позицию, обозначенную цифрой.
|
ФОРМУЛЫ ВЕЩЕСТВ |
РЕАГЕНТ |
А) HNO3 и NaNO3 Б) KCI и NaOH В) NaCI и BaCI2 Г) AICI3 и MgCI2 |
1) Cu 2) KOH 3) HCI 4) KNO3 5) CuSO4 |
Ответ: А) Даны два вещества, кислота и соль. Азотная кислота является сильным окислителем и взаимодействует с металлами, стоящими в электрохимическом ряду напряжений металлов как до водорода, так и после, причем взаимодействует как концентрированная, так и разбавленная. Например, азотная кислота HNO3 взаимодействует с медью с образованием соли меди, воды и оксида азота. При этом, помимо выделения газа, раствор приобретает характерную для солей меди синюю окраску, например:
8HNO3(р) + 3Cu = 3Cu(NO3)2 + 2NO + 4H2O,
а соль NaNO3 с медью не реагирует. Ответ 1.
Б) Даны соль и гидроксид активных металлов, у которых практически все соединения растворимы в воде, поэтому выбираем вещество из колонки реагентов, которое при взаимодействии с одним из данных веществ выпадает в осадок. Этим веществом будет сульфат меди. С хлоридом калия реакция не пойдет, а вот с гидроксидом натрия выпадет красивый синий осадок, по уравнению реакции:
CuSO4 + 2NaOH = Cu(OH)2 + Na2SO4.
Ответ 5.
В) Даны две соли, хлориды натрия и бария. Если все соли натрия растворимы, то с солями бария наоборот – многие соли бария нерастворимы. По таблице растворимости определяем, что сульфат бария нерастворим, поэтому реактивом будет сульфат меди. Ответ 5.
Г) Опять даны 2 соли – AlCl3 и MgCl2 – и опять хлориды. При сливании данных растворов с HCl, KNO3 CuSO4 не образуют никаких видимых изменений, c медью вообще не реагируют. Остается КOH. С ним обе соли выпадают в осадок, с образованием гидроксидов. Но гидроксид алюминия – амфотерное основание. При добавлении избытка щелочи осадок растворяется с образованием комплексной соли. Ответ 2.
Общий ответ на данное задание выглядит так:
|
А |
Б |
В |
Г |
|
1 |
5 |
5 |
2 |
Задание 26
Установите соответствие между веществом и основной областью его применения: к каждой позиции, обозначенной буквой, подберите соответствующую позицию, обозначенную цифрой.
|
ВЕЩЕСТВО |
ОБЛАСТЬ ПРИМЕНЕНИЯ |
A) метан Б) изопрен В) этилен |
1) получение капрона 2) в качестве топлива 3) получение каучука 4) получение пластмасс |
Ответ: А) Метан при сгорании выделяет большое количество тепла, поэтому его можно использовать в качестве топлива (ответ 2).
Б) Изопрен, являясь диеновым углеводородом, при полимеризации образует каучук, который затем превращают в резину (ответ 3).
В) Этилен – непредельный углеводород, который вступает в реакции полимеризации, поэтому может быть использован в качестве пластических масс (ответ 4).
Итого:
|
А |
Б |
В |
|
2 |
3 |
4 |
Задание 27
Вычислите массу нитрата калия (в граммах), которую следует растворить в 150,0 г. раствора с массовой долей этой соли 10% для получения раствора с массовой долей 12%. (Запишите число с точностью до десятых).
Решим данную задачу:
1. Определим массу нитрата калия, содержащуюся в 150 г 10% раствора. Воспользуемся волшебным треугольником:
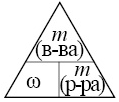
Отсюда масса вещества равна: ω · m(р-ра) = 0,1 · 150 = 15 г.
2. Пусть масса добавленного нитрата калия равна x г. Тогда масса всей соли в конечном растворе будет равна (15 + x) г, масса раствора (150 + x), а массовую долю нитрата калия в конечном растворе можно записать как: ω(KNO3) = 100% – (15 + x)/(150 + x)
Далее, по условию задачи известно, что конечный раствор должен иметь ω(KNO3) = 12%
100% – (15 + x)/(150 + x) = 12%
(15 + x)/(150 + x) = 0,12
15 + x = 18 + 0,12x
0,88x = 3
x = 3/0,88 = 3,4
Ответ: Для получения 12% раствора соли необходимо добавить 3,4 г KNO3.

Задание 28
В результате реакции, термохимическое уравнение которой
2H2(г) + O2(г) = H2O (г) + 484 кДж,
выделилось 1452 кДж теплоты. Вычислите массу образовавшейся при этом воды (в граммах).
Данная задача может быть решена в одно действие.
Согласно уравнению реакции, в результате ее образовалось 36 граммов воды и выделилось 484 кДж энергии. А 1454 кДж энергии выделится при образовании Х г. воды.
| Х = | 36 г · 1452 кДж | = 108 г |
| 484 кДж |
Ответ: При выделении 1452 кДж энергии образуется 108 г воды.
Задание 29
Вычислите массу кислорода (в граммах), необходимого для полного сжигания 6,72 л (н.у.) сероводорода.
Для решения данной задачи напишем уравнение реакции горения сероводорода и рассчитаем массы кислорода и сероводорода, вступивших в реакцию, по уравнению реакции
| 2H2S | + | 3O2 | = 2SO2 + 2H2O |
|
Mr
= 34 M = 34г/моль n = 2 моль m = 68 г |
|
Mr = 32 M = 32г/моль n = 3 моль m = 96 г |
|
1. Определяем количество сероводорода, содержащегося в 6,72 л.
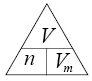
| n(H2S) = | V | = | 6,72 | = 0,3 моль |
| Vm | 22,4 |
2. Определяем количество кислорода, которое прореагирует с 0,3 моль сероводорода.
По уравнению реакции, с 2 моль H2S реагирует 3 моль O2.
По уравнению реакции, с 0,3 моль H2S прореагирует с Х моль О2.
Отсюда Х = 0,45 моль.
3. Определим массу 0,45 моль кислорода
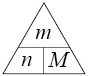
m(O2) = n · M = 0,45 моль · 32 г/моль = 14,4 г.
Ответ: масса кислорода равна 14,4 грамма.
Задание 30
Из предложенного перечня веществ (перманганат калия, гидрокарбонат калия, сульфит натрия, сульфат бария, гидроксид калия) выберите вещества, между которыми возможна окислительно-восстановительная реакция. в ответе запишите уравнение только одной из возможных реакций. Составьте электронный баланс, укажите окислитель и восстановитель.
Ответ: КMnO4 – известный окислитель, окисляет вещества, содержащие элементы в низшей и промежуточной степенях окисления. Его действия могут проходить в нейтральной, кислой и щелочной средах. При этом марганец может восстанавливаться до различных степеней окисления: в кислой среде – до Mn2+, в нейтральной среде – до Mn4+, в щелочной среде – до Mn6+. В сульфите натрия содержится сера в степени окисления 4+, которая может окислиться до 6+. И наконец, гидроксид калия определит реакцию среды. Пишем уравнение данной реакции:
KMnO4 + Na2SO3 + KOH = K2MnO4 + Na2SO4 + H2O
Далее составляем схему окислительно-восстановительного процесса и расставляем коэффициенты.
Mn7+ + 1e → = Mn6+ S4+ –2e → = S6+ |
2 процесс восстановления, окислитель 1 процесс окисления, восстановитель |
После расставления коэффициентов формула приобретает следующий вид:
2KMnO4 + Na2SO3 + 2KOH = 2K2MnO4 + Na2SO4 + H2O
Следовательно, KMnO4 – является окислителем, а Na2SО3 – восстановителем.

Задание 31
Из предложенного перечня веществ (перманганат калия, гидрокарбонат калия, сульфит натрия, сульфат бария, гидроксид калия) выберите вещества, между которыми возможна реакция ионного обмена. В ответе запишите молекулярное, полное и сокращенное ионное уравнение только одной из возможных реакций.
Ответ: Рассмотрим реакцию обмена между гидрокарбонатом калия и гидроксидом калия
KHCO3 + KOH = K2CO3 + H2O
Если в результате реакции в растворах электролитов образуется нерастворимое или газообразное, или малодиссоциирующее вещество, то такая реакция протекает необратимо. В соответствии с этим данная реакция возможна, так как один из продуктов реакции (Н2О) – малодиссоциирующее вещество. Запишем полное ионное уравнение.
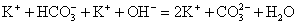
Так как вода – малодиссоциирующее вещество, она пишется в виде молекулы. Далее составляем сокращенное ионное уравнение. Те ионы, которые перешли из левой части уравнения в правое, не изменяя знака заряда, вычеркиваем. Остальное переписываем в сокращенное ионное уравнение.
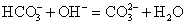
Это уравнение и будет ответом на данное задание.
Задание 32
При электролизе водного раствора нитрата меди(II) получили металл. Металл обработали концентрированной серной кислотой при нагревании. Выделяющийся в результате газ прореагировал с сероводородом с образованием простого вещества. Это вещество нагрели с концентрированным раствором гидроксида калия. Напишите уравнения четырех описанных реакций.
Ответ: Электролиз – это окислительно-восстановительный процесс, проходящий на электродах при пропускании постоянного электрического тока через раствор или расплав электролита. В задании говорится об электролизе раствора нитрата меди. При электролизе растворов солей вода также может принимать участие в электродных процессах. При растворении соли в воде она распадается на ионы:
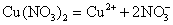
На катоде происходят процессы восстановления. В зависимости от активности металла, могут восстанавливаться металл, металл и вода. Так как медь в электрохимическом ряду напряжений металлов стоит правее водорода, то на катоде будет восстанавливаться медь:
Cu2+ + 2e = Cu0.
На аноде будет происходить процесс окисления воды.
Медь не реагирует с растворами серной и соляной кислот. Но концентрированная серная кислота является сильным окислителем, поэтому может реагировать с медью по следующему уравнению реакции:
Cu + 2H2SO4(конц.) = CuSO4 + SO2 + 2H2O.
Сероводород (H2S) содержит серу в степени окисления 2–, поэтому выступает в роли сильного восстановителя и восстанавливает серу в оксиде серы IV до свободного состояния
2H2S + SO2 = 3S + 2H2O.
Образующееся вещество, сера, взаимодействует с концентрированным раствором гидроксида калия при нагревании с образованием двух солей: сульфида и сульфита серы и воды.
S + KOH = K2S + K2SO3 + H2O
Задание 33
Напишите уравнения реакций, с помощью которых можно осуществить следующие превращения:

При написании уравнений реакций используйте структурные формулы органических веществ.
Ответ: В данной цепочке предложено выполнить 5 уравнений реакций, по числу стрелочек между веществами. В уравнении реакции № 1 серная кислота играет роль водоотнимающей жидкости, поэтому в результате ее должен получиться непредельный углеводород.

Следующая реакция интересна тем, что протекает по правилу Марковникова. По этому правилу, при соединении галогеноводородов к несимметрично построенным алкенам, галоген присоединяется к менее гидрированному атому углерода при двойной связи, а водород, наоборот.
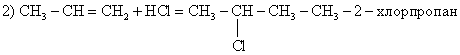
В следующем уравнении реакции, атом хлора замещается на группу –ОН

В уравнении реакции № 4 в качестве продукта должен получиться пропен, исходя из условия задания (в обоих случаях в качестве продукта стоит Х1). Условия реакции будут также одинаковыми.

В последнем уравнении реакции предлагается окислить пропен перманганатом калия в нейтральной среде при низкой температуре.
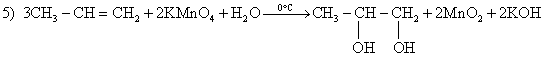

Задание 34
При нагревании образца карбоната кальция часть вещества разложилась. При этом выделилось 4,48 л (н.у.) углекислого газа. Масса твердого остатка составила 41,2 г. Этот остаток добавили к 465,5 г раствора хлороводородной кислоты, взятой в избытке. Определите массовую долю соли в полученном растворе.
В ответе запишите уравнения реакций, которые указаны в условии задачи, и приведите все необходимые вычисления (указывайте единицы измерения искомых величин).
Ответ: Запишем краткое условие данной задачи.
Дано: V(CO2) = 4,48 л m() = 41,2 г. m(HCl) = 465,5 г |
Решение: Напишем уравнение первой реакции разложения карбоната кальция.
|
|||||||||||||||
Найти: ω% (СaCl2) |
После того как все приготовления приведены, приступаем к решению.
1) Определяем количество СО2, содержащееся в 4,48 л. его.
n(CO2) = V/Vm = 4,48 л / 22,4 л/моль = 0,2 моль
2) Определяем количество образовавшегося оксида кальция.
По уравнению реакции образуется 1 моль СО2 и 1 моль СаО
Следовательно: n(CO2) = n(CaO) и равняется 0,2 моль
3) Определяем массу 0,2 моль СаО
m(CaO) = n(CaO) · M(CaO) = 0,2 моль · 56 г/моль = 11,2 г
Таким образом, твердый остаток массой 41,2 г состоит из 11,2 г СаО и (41,2 г. – 11,2 г.) 30 г СаСО3
4)
Определим количество СаСО3, содержащееся в 30 г
n(CaCO3) = m(CaCO3) / M(CaCO3) = 30 г / 100 г/моль = 0,3 моль
Далее пишем следующие два уравнения необходимые для решения данной.
Задачи:
CaO + HCl = CaCl2 + H2O
CaCO3 + HCl = CaCl2 + H2O + CO2
5) Определим количество хлорида кальция, образующееся в результате данных реакций.
В реакцию вступило 0,3 моль CaCO3 и 0,2 моль СаО всего 0,5 моль.
Соответственно, образуется 0,5 моль CaCl2
6) Рассчитаем массу 0,5 моль хлорида кальция
M(CaCl2) = n(CaCl2) · M(CaCl2) = 0,5 моль · 111 г/моль = 55,5 г.
7) Определяем массу углекислого газа. В реакции разложения участвовало 0,3 моль карбоната кальция, следовательно:
n(CaCO3) = n(CO2) = 0,3 моль,
отсюда:
m(CO2) = n(CO2) · M(CO2) = 0,3 моль · 44г/моль = 13,2 г.
8) Находим массу раствора. Она состоит из массы соляной кислоты + масс твердого остатка (CaCO3 + CaO) минут масса выделившегося CO2. Запишем это в виде формулы:
m(р-ра) = m(CaCO3 + CaO) + m(HCl) – m(CO2) = 465,5 г + 41,2 г – 13,2 г = 493,5 г.
9) И наконец, ответим на вопрос задачи. Найдем массовую долю в % соли в растворе, воспользовавшись следующим волшебным треугольником:

ω%(CaCI2) = m(CaCI2) / m(р-ра) = 55,5 г / 493,5 г = 0,112 или 11,2%
Ответ: ω % (СaCI2) = 11.2%
Задание 35
Органическое вещество А содержит 11,97% азота, 9,40% водорода и 27,35% кислорода по массе и образуется при взаимодействии органического вещества Б с пропанолом-2. Известно, что вещество Б имеет природное происхождение и способно взаимодействовать как с кислотами, так и со щелочами.
На основании данных условия выполните задания:
1) Проведите необходимые вычисления (указывайте единицы измерения искомых физических величин) и установите молекулярную формулу исходного органического вещества;
2) Составьте структурную формулу этого вещества, которая однозначно покажет порядок связи атомов в его молекуле;
3) Напишите уравнение реакции получения вещества А из вещества Б и пропанола-2 (используйте структурные формулы органических веществ).
Ответ: Давайте постараемся разобраться с данной задачей. Напишем краткое условие:
Дано: ω(N) = 11,97% ω(H) = 9,40% ω(O) = 27,35% |
Решение: 1) Находим % углерода, так как углерод постоянный элемент органических веществ. Массовая доля в % всех элементов в любом соединении равняется 100%, поэтому вычтем из 100% массовые доли всех данных в задаче элементов. Цифра, которая у нас получится, и будет отражать массовую долю углерода. |
Найти: CxHyOzNm - ? |
ω(C) = 100% – 11,97% – 9,40% – 27,35% = 51,28% (ω(C) = 51,28%)
2) Зная массовые доли всех элементов, входящих в состав молекулы, можем определить ее молекулярную формулу.
Примем массу вещества А за 100 г. Тогда в массы всех элементов, входящих в его состав, будут равны: m(C) = 51,28 г; m(N) = 11,97 г; m(H) = 9,40 г; m(O) = 27,35 г. Определим количество каждого элемента:
n(C) = m(C) · M(C) = 51,28 г / 12 г/моль = 4,27 моль
n(N) = m(N) · M(N) = 11,97 г / 14 г/моль = 0,855 моль
n(H) = m(H) · M(H) = 9,40 г / 1 г/моль = 9,40 моль
n(O) = m(O) · M(O) = 27,35 г / 16 г/моль = 1,71 моль
Далее разделим все эти цифры на наименьшее число (0,855), чтобы получить целочисленные значения количества атомов; получим;
x : y : z : m = 5 : 1 : 11 : 2.
Таким образом молекулярная формула вещества А равна: C5H11O2N.
3) Попробуем составить структурную формулу вещества А. Мы уже знаем, что углерод в органической химии всегда четырехвалентен, водород – одновалентен, кислород двухвалентен и азот трехвалентен. В условии задачи также сказано, что вещество Б способно взаимодействовать как с кислотами, так и со щелочами, то есть оно амфотерно. Из природных амфотерных веществ нам известно, что аминокислоты обладают выраженной амфотерностью. Следовательно можно предположить, что вещество Б относится к аминокислотам. Ну и конечно, берем во внимание, что оно получается при взаимодействии с пропанолом-2. Посчитав количество атомов углерода в пропаноле-2, можно сделать смелый вывод, что вещество Б – аминоуксусная кислота. После некоторого количества попыток, получилась следующая формула:

4) В заключение напишем уравнение реакции взаимодействия аминоуксусной кислоты с пропанолом-2.