Химические свойства аммиака. Химия. 8 класс. Конспект урока
УМК «Химия. 9 класс» О. В. Габриеляна.
Тип урока:урок «открытия» нового знания.
Цели урока: установить причинно-следственные связи между строением молекулы аммиака и его свойствами, расширить представления об основаниях на примере раствора аммиака, воспитание ответственного отношения к учебной деятельности.
Задачи урока:
Воспитательные:
- совершенствовать навыки делового сотрудничества в процессе решения проблемы, работы в группе;
- формировать положительную мотивацию учебной деятельности.
Развивающие:
- развивать умение работать с электронными образовательными ресурсами разного типа, планировать решение проблемы и выстраивать цепочку действий, проводить аналогии.
Образовательные:
- объяснить причины основных свойств водного раствора аммиака;
- изучить механизм образования донорно-акцепторной связи на примере образования иона аммония;
- определить окислительно-восстановительные свойства аммиака и объяснить их причину.
Методы обучения: по источнику знаний (словесные, наглядные, практические), по характеру деятельности обучающихся (проблемное изложение, частично-поисковый).
Приемы обучения: постановка проблемных вопросов, проведение эксперимента для получения нужной информации, работа с электронными образовательными ресурсами.
Средства обучения: компьютер, проектор, электронные образовательные ресурсы, инструктивные карты.
Ожидаемые результаты
Личностные: ответственное отношение к труду, целеустремлённость, умение управлять собственной познавательной деятельностью.
Метапредметные: применение основных методов познания (системно-информационного анализа), использование основных интеллектуальных операций (формулирование гипотез, анализ, синтез, сравнение, обобщение, выявление причинно-следственных связей).
Предметные:
- Учащиеся должны знать: механизм образования ковалентной связи в молекуле аммиака и катионе аммония, химические свойства аммиака.
- Учащиеся должны уметь: давать определение понятию донорно-акцепторный механизм образования ковалентной связи, описывать простое вещество – азот и сложное вещество – аммиак, записывать уравнения химических реакций, характеризующие свойства аммиака, наблюдать и описывать демонстрируемые химические эксперименты, делать выводы и умозаключения из наблюдений, структурировать изученный материал, фиксировать его в рабочей тетради.
Оборудование и реактивы для учителя: раствор соляной кислоты, раствор аммиака, 2 колбы с пробками, индикатор лакмус.
Оборудование и реактивы для учащихся: раствор аммиака, пробирка с пробкой, универсальная индикаторная бумага.
Перечень электронных образовательных ресурсов
|
№ |
Название ресурса |
Тип, вид ресурса |
Форма предъявления информации |
Гиперссылка на ресурс, обеспечивающий доступ к ЭОР |
|
1 |
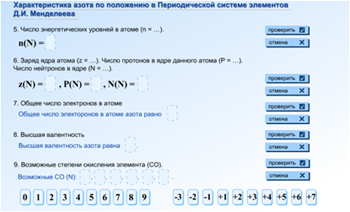
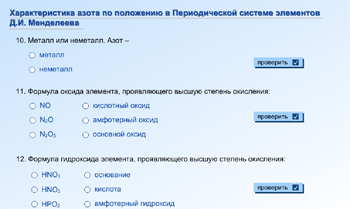
Характеристика азота по положению в Периодической системе элементов Д. И. Менделеева (N 125267) |
Контролирующий |
Интерактивное задание |
http://files.school-collection.edu.ru/dlrstore/bed08f98-8cff-11db-b606-0800200c9a66/ch09_24_01.swf |
|
2 |
Донорно-акцепторный механизм образования катиона аммония (N 125254) |
Информационный |
Анимация |
|
|
3 |
Химические свойства аммиака |
Информационный |
Информационный модуль |
http://fcior.edu.ru/card/213/fizicheskie-i-himicheskie-svoystva-ammiaka.html |
|
4 |
Тренажёр «Химические свойства аммиака» |
Практический |
Интерактивное задание |
Технологическая карта урока
|
Этап урока |
Содержание |
Деятельность учителя |
Деятельность обучающихся |
Планируемый результат |
|
1. Мотивация (самоопределение) к учебной деятельности |
Приветствие обучающихся, проверка готовности к уроку. Обращение к классу: При активном включении в групповую и фронтальную работу вы сможете:
|
Сообщает обучающимся о видах деятельности на уроке и возможных результатах этой деятельности. |
Подготовка к активной учебно-познавательной деятельности. |
Развитие личностных УУД: самоопределение; смыслообразование; внутренней позиции обучающегося; учебно-познавательной мотивации. |
|
2. Актуализация знаний |
Работа с электронным образовательным ресурсом Характеристика азота по положению в ПСХЭ Д.И. Менделеева
|
Организация работы с ЭОР контролирующего типа. |
Работа с электронным образовательным ресурсом (3 слайда) (3 капитана по одному от каждого ряда, фронтально работают с представителями своей команды при выполнении интерактивного задания на одном из 3-х слайдов, согласно жеребьёвке) |
Развитие личностных УУД: осознание ответственности за общее дело Развитие познавательных УУД: структурирование знаний; использование знаково-символических средств; построение речевого высказывания в устной форме. Развитие коммуникативных УУД: учет разных мнений, координирование в сотрудничестве разных позиций. |
|
3. Фиксирование индивидуального затруднения в пробном действии. |
Сегодня на уроке мы будем рассматривать водородное соединение азота. Для создания проблемной ситуации, ученикам предлагается вспомнить, что им известно о свойствах растворов водородных соединений неметаллов VI и VII групп, а также сравнить окраску индикатора лакмуса в водных растворах водородных соединений хлора и азота. Что удивило? Что предполагали увидеть? |
Побуждает к осознанию противоречия между имеющимися знаниями и наблюдаемыми результатами. |
Отвечают на вопросы учителя. В ходе демонстрационного опыта наблюдают разную окраску лакмуса. Обсуждают увиденные результаты. |
Развитие познавательных УУД: анализ, сравнение, аналогии. |
|
4. Выявление места и причины затруднения |
Какую реакцию среды имеет водный раствор аммиака? Лабораторный опыт «Определение среды раствора аммиака с помощью универсальной индикаторной бумаги» |
Организует практическую деятельность. |
Выполняют (парами) лабораторный опыт, делают вывод. |
Развитие личностных УУД: учебно-познавательный интерес; смыслообразование. регулятивных УУД: волевая саморегуляция. познавательных УУД: анализ, сравнение, подведение под понятие. коммуникативных УУД: формулирование и аргументация своего мнения и позиции в коммуникации. |
|
Проблемная ситуация:почему растворы имеют разную среду, хотя оба образованны атомами неметаллов? |
Задает проблемную ситуацию. |
Высказывают предположения (разное строение атомов хлора и азота). |
||
|
5. Построение и реализация проекта выхода из затруднения
|
Работа групп (4 человека) с инструктивной картой №1 Инструктивная карта № 1 1. Составьте электронно-графические формулы: а) атома водорода; б) катиона водорода; в) атома азота. 2. Составьте схему образования молекулы водородного соединения азота. 3. На основании изменения окраски индикатора в водном растворе аммиака, предположите, соединение какого класса образуется в результате проведённой реакции. Составьте уравнение химической реакции между аммиаком и водой. 4. Установите причину появления в растворе гидроксид-ионов. 5. Определите, какой ещё ион образуется в растворе? |
Организация работы групп с инструктивной картой №1 |
Работа групп с инструктивной картой №1 |
Развитие личностных УУД: осознание ответственности за общее дело регулятивных УУД: волевой саморегуляции; познавательной инициативы; прогнозирования. познавательных УУД: познавательная инициатива, построение логической цепи рассуждений; использование знаково-символических средств; построение речевых высказываний; установление причинно-следственных связей. Коммуникативных УУД: планирование учебного сотрудничества; формулирование и аргументация своего мнения и позиции в коммуникации; понимание относительности мнений и подходов для решения проблем; адекватное использование речи для планирования и регуляции своей деятельности. |
|
Все ли задания вы смогли выполнить? В чем затруднения? Проблема: За счет чего аммиак может вступать в реакции присоединения, если все неспаренные электроны использованы на связи с водородом? |
|
Самопроверка. |
||
|
Инструктивная карта № 2
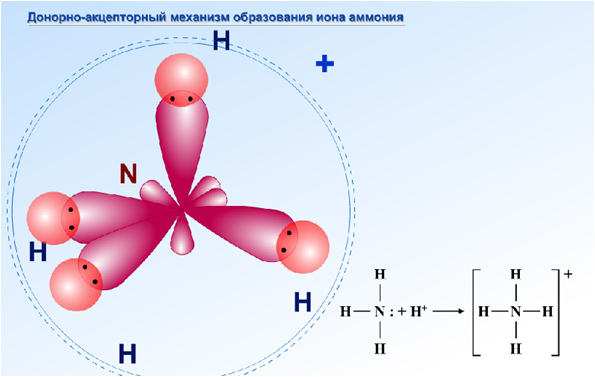
«Механизмы образования ковалентной связи» Атом азота имеет 5 электронов на внешнем энергетическом уровне, из них 2 спаренных электрона и 3 – неспаренных. Атом азота за счёт трёх неспаренных электронов образует ковалентную полярную связь с тремя атомами водорода в результате образования общих электронных пар по обменному механизму. Неподелённая электронная пара атома азота может участвовать в образовании четвёртой ковалентной связи. При этом атом азота выполняет роль донора двух спаренных электронов. Катион водорода имеет свободную s-орбиталь, на которую он может принимать электронную пару азота, то есть выполнять роль акцептора. Указанный процесс происходит при образовании катиона аммония. |
Организация работы групп с инструктивной картой № 2 |
Работа групп с инструктивной картой № 2, выполнение задания на листах ватмана маркерами. |
||
|
Проверка в ходе работы с электронным образовательным ресурсом Донорно-акцепторный механизм образования связи
|
Организация взаимо- и самопроверки. |
Проверка с использованием ЭОР. |
||
|
Существуют ли вещества, которые взаимодействуют с аммиаком подобно воде? Составьте уравнение реакции взаимодействия аммиака с соляной и серной кислотой. Проверка с использованием ЭОР Почему в отличие от азота аммиак в окислительно-восстановительных процессах может быть только восстановителем? |
Формулирует проблему |
Самостоятельно составляют уравнения реакций аммиака с соляной и серной кислотой. (2 человека работают у доски) |
||
|
Работа групп с инструктивной картой № 3. (с использованием ЭОР Химические свойства аммиака)
Инструктивная карта № 3 1. Определите степень окисления атома азота в молекуле аммиака. 2. В какой роли может выступать аммиак в окислительно-восстановительных процессах? 3. Познакомьтесь с окислительно-восстановительными свойствами аммиака в ходе работы с информационным электронным образовательным ресурсом «Химические свойства аммиака»: а) Познакомьтесь с видеофрагментом «Горение аммиака»
б) Познакомьтесь с видеофрагментом «Каталитическое окисление аммиака»
|
Формулирует проблему: Организация групповой работы |
Работают с инструктивной картой №3 |
||
|
5. Первичное закрепление |
Приём «Проверь себя»
|
Организация индивидуальной работы в тетради |
Индивидуальная работа в тетради с текстом задания ЭОР. Проверка результатов работы (сравнение с эталоном), самооценка. |
Развитие личностных УУД: осознание ответственности за индивидуальную работу. регулятивных УУД: волевая саморегуляция; контроль; коррекция. познавательных УУД: подведение под понятие; использование знаково-символических средств; самостоятельный учет установленных ориентиров действия в новом учебном материале. коммуникативных УУД: планирование учебного сотрудничества в случае затруднений |
|
6. Рефлексия учебной деятельности на уроке |
Что нового вы узнали на уроке? Узнали, что водный раствор аммиака, в отличие от аналогичных растворов неметаллов VI и VII групп, проявляет основные свойства; – механизм образования донорно-акцепторной связи; – выяснили, что в ОВР аммиак может быть только восстановителем. Как бы вы сформулировали тему урока? |
Составляет кластер, используя ответы обучающихся. |
Отвечают на вопросы учителя Тема урока “Аммиак и его свойства” формулируется учащимися в конце урока. |
Развитие личностных УУД:самооценка на основе критерия успешности; адекватное понимание причин успеха / неуспеха в учебной деятельности. Познавательных УУД: контроль и оценка процесса и результатов деятельности; Коммуникативных УУД: формулирование и аргументация своего мнения. |
|
7. Д/З |
Д/з: Составить инструктивную карту к практической работе, используя различные источники информации. Лабораторная работа "Получение аммиака, свойства аммиака", познакомиться с правилами безопасности при работе с аммиаком Правила безопасной работы с аммиаком |
Комментирует домашнее задание |
Фиксация домашнего задания в тетради. |
|