Углерод. Химия. 9 класс. Конспект урока
Класс: 9.
Автор УМК: Габриелян О.С.
Тип урока: урок изучения нового материала.
Вид урока: смешанный
Цель урока. Обеспечить усвоение учащимися на уровне восприятия, осмысления и первичного запоминания знаний состава, строения, свойств и применения углерода; закрепить знания обучающихся об аллотропии. Формирование базовых компетентностей современного человека: учебно-познавательной, информационной, коммуникативной, личностного совершенствования.
Задачи урока:
- Образовательные: повторить строение атома и аллотропию на примере углерода. Рассмотреть строение, сравнение свойств и применение алмаза и графита. Познакомить учащихся с явлением адсорбции и его практическом значении. Изучить химические свойства углерода. Рассмотреть круговорот углерода в природе.
- Развивающие: развивать у учащихся умения сравнивать и анализировать теоретические сведения, применять их на практике, делать выводы; развивать логическое мышление.
- Воспитательные: формировать естественно - научное мировоззрение; информационную культуру; чувство патриотизма на примере научной деятельности русских ученых – химиков (Ловиц Т.Е., Зелинского Н.Д.); бережного отношения к природным ресурсам.
Материально-техническое обеспечение урока: компьютеры; учебник-навигатор химия 9 класс издательства «Дрофа»; мультимедийный проектор и экран.
Оборудование и реактивы. Периодическая таблица химических элементов Д.И.Менделеева. Модели кристаллических решеток алмаза и графита, иллюстрации с картин В. Боровиковского и фотографии сокровищ Алмазного фонда, образцы изделий из графита (карандаши, электроды и др.) и сажи (тушь, краски, резина и др.), древесный уголь, таблетки карболена, растворы чернил, вишневого компота, сока свеклы; одеколон. Стеклянная трубка диаметром 1,5–2 см (или пробирка с дырявым дном), штатив, вата, речной песок, стакан, колба, прибор для восстановления меди из оксида меди, противогаз, кукурузные палочки, пипетка.
Межпредметные и внутрипредметные связи.
Межпредметная связь с предметами: искусство, география, физика, биология, экология, ОБЖ, геометрия.
Внутрипредметные связь:
- химия 8 класс – строение атома, химические связи, способы очистки веществ, аллотропия, кристаллические решетки, окислительно-восстановительные свойства;
- химия 9 класс – получение и химическое свойства металлов, химические элементы в клетках живых организмов;
- химия 10 класс – строение атома углерода, получение метана, природные источники углеводородов;
- химия 11 класс – валентные возможности атомов химических элементов, неметаллы.
Ход урока
I. Организационный момент
Приветствие. Проверка готовности учащихся к учебным занятиям.
II. Актуализация знаний
Учитель выразительно читает стихотворение:
Из меня состоит все живое,
Я – графит, антрацит и алмаз,
Я на улице, в школе и в поле,
Я в деревьях и в каждом из вас.
Учитель: о каком химическом элементе идет речь в этом стихотворении?
Угадывая название элемента, учащиеся называют тему урока и вместе с учителем формулируют его цель.
Цель урока:
- Изучить строение атома углерода, опираясь на положение в таблице Менделеева;
- Рассмотреть аллотропные модификации углерода;
- Изучить химические свойства углерода и познакомиться с его применением.
III. Изучение нового материала
1. Строение и свойства атомов
Учитель: охарактеризуйте строение атома углерода на основании его положения в Периодической системе химических элементов, ответив на вопросы и используя материал электронного учебника:
- Каков химический знак углерода?
- Положение в периодической системе Д.И.Менделеева (номер периода и его вид, номер группы и тип подгруппы, номер элемента).
- Каков заряд ядра?
- Какова атомная масса?
- Сколько протонов в ядре атома?
- Сколько нейтронов в ядре атома?
- Сколько электронов в атоме углерода?
- Электронная формула атома.
- Чему равна высшая степень окисления?
- Чему равна низшая степень окисления?
- Какие свойства будет проявлять углерод, вступая в химическое взаимодействие?
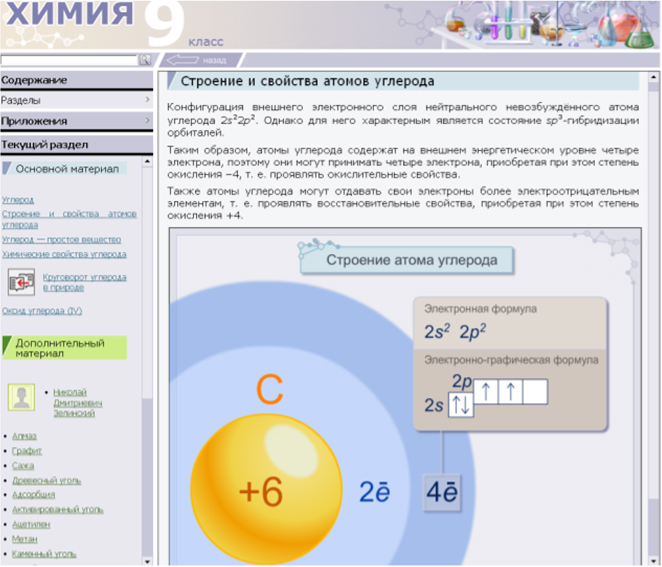
Учащиеся характеризуют положение углерода в ПСХЭ,
определяют его порядковый номер и составляют электронную формулу атома, делают соответствующую запись в тетради:
- химический знак – С
- второй период малый, IV группа, главная подгруппа, номер элемента – 6
- заряд ядра +6
- Ar(C) = 12
- 6 протонов
- 6 нейтронов
- 6 электронов
- +6С 2 e 4 e
- высшая степень окисления +4
- низшая степень окисления –4
Исходя из строения атома, прогнозируют окислительно-восстановительные свойства углерода:
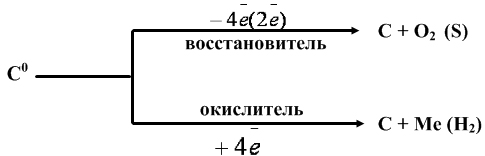
2. Аллотропия
Учитель: Почему углерод – это графит, антрацит и алмаз?
Учащиеся: Углерод образует несколько простых веществ.
Учитель: Как называется такое явление?
Учащиеся: аллотропия – способность атомов одного химического элемента образовывать несколько простых веществ. Эти простые вещества называются – аллотропными видоизменениями или модификациями.
Учитель: каковы причины аллотропии углерода?
Учащиеся: различное строение кристаллических решеток.
Учитель демонстрирует модели решеток алмаза и графита и предлагает учащимся заполнить таблицу «Аллотропные модификации углерода», предварительно ознакомившись с материалом электронного учебника.
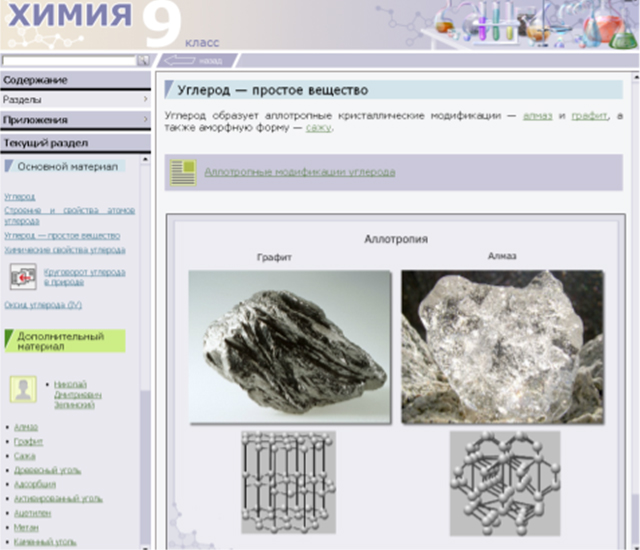
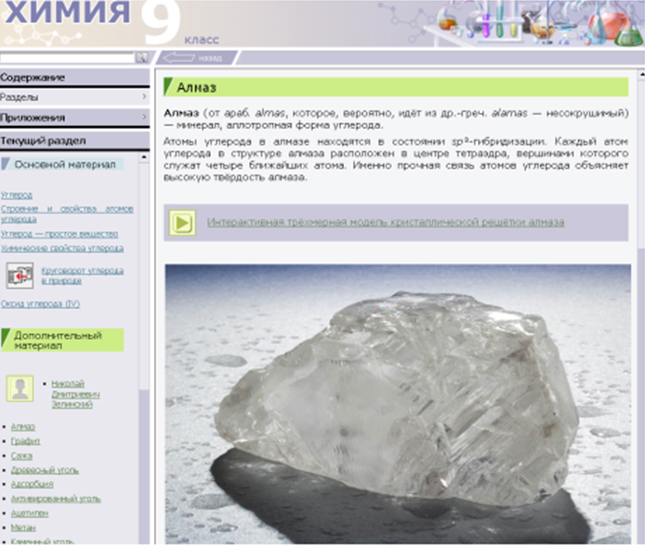
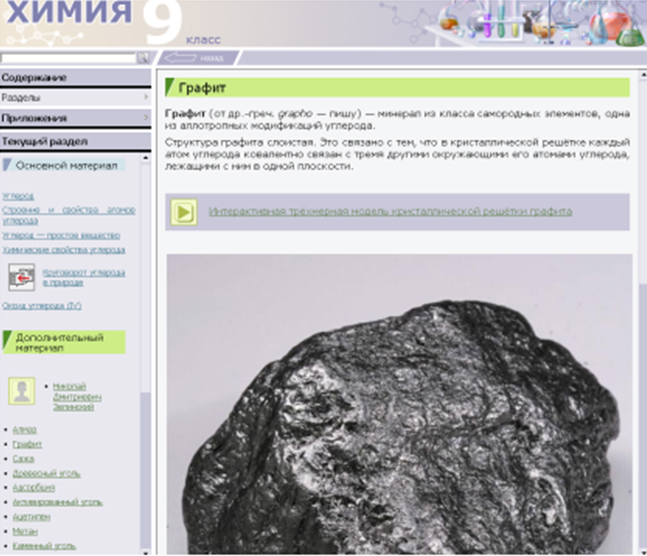
«Аллотропные модификации углерода»
|
Признаки сравнения |
Алмаз |
Графит |
|
Сходство |
||
|
Качественный состав |
|
|
|
Тип вещества |
|
|
|
Физические свойства |
|
|
|
Различия |
||
|
Кристаллическая решетка |
|
|
|
Физические свойства |
|
|
|
Применение |
|
|
Заполнив таблицу, учащиеся слушают выступления одноклассников с дополнительной информацией об алмазах, демонстрацией иллюстрации с картин В. Боровиковского и фотографий сокровищ Алмазного фонда.
Учитель: кроме алмаза и графита, углерод образует и другие аллотропные модификации – это карбин, фуллерен.
Сообщения учащихся о карбине и фуллерене.
Учащиеся под руководством учителя обобщают полученные знания.
Углерод образует аллотропные модификации: алмаз, графит, карбин, фуллерен. Причина этого явления состоит в разном строении кристаллических решеток:
1) алмаз имеет объемную тетраэдрическую атомную решетку;
2) графит – плоскостную атомную кристаллическую решетку;
3) карбин – линейную;
4) фуллерен – сферическую.
Учитель: сходное строение с графитом имеют сажа и древесный уголь.
Учащиеся работают с дополнительным материалом электронного учебника.
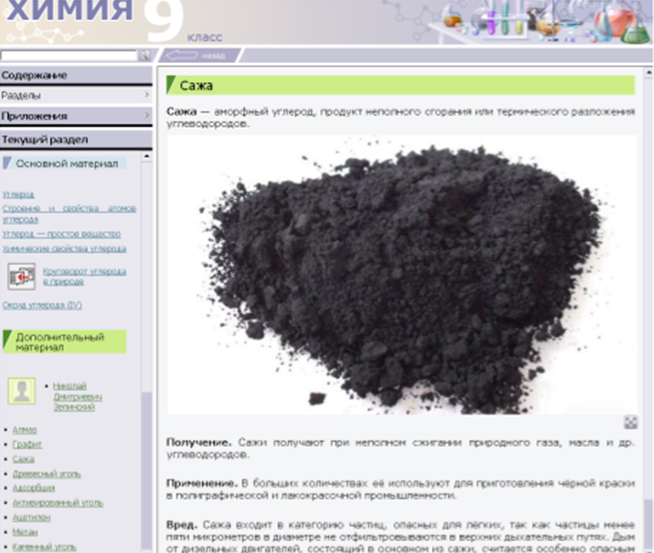
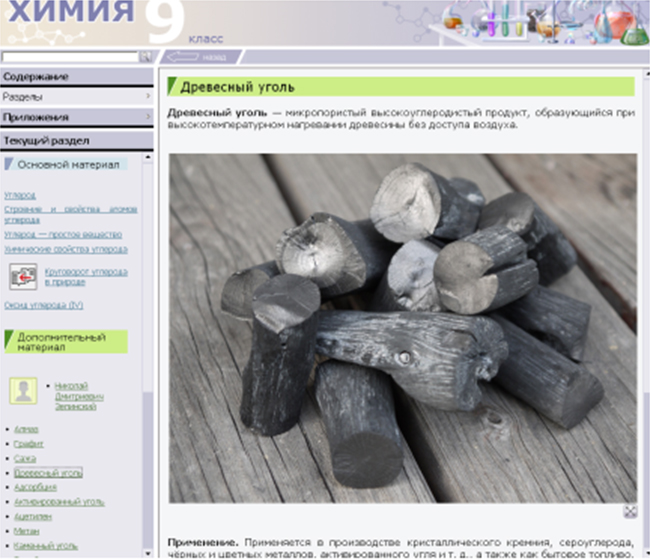
3. Адсорбция
Учитель демонстрирует древесный уголь и таблетки карболена (активированный уголь). Что общего между ними?
Учащиеся отвечают, что и древесный уголь и активированный уголь обладают способностью поглощать газы и растворенные вещества – адсорбцией.
Учитель демонстрирует адсорбционные свойства угля (приложение 1).
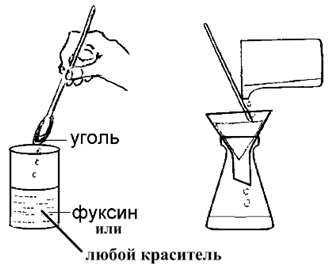
Рассказывает, что открытое русским химиком Ловицем явление адсорбции широко используется для очистки сахара на рафинадных заводах от веществ, придающих ему желтый цвет; для очистки спирта.
На поглотительной способности активированного угля также основано и действие противогазов – устройства для защиты от вредных примесей, имеющихся в воздухе. Первый противогаз был изобретен Н.Д.Зелинским и спас жизнь тысячам солдат в период Первой мировой войны.
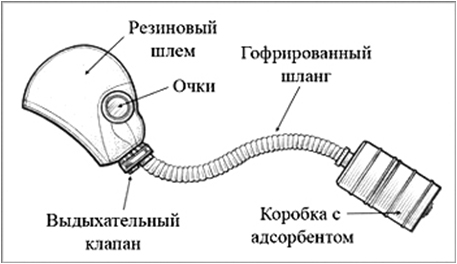
Учащиеся знакомятся с биографией ученого по дополнительному материалу из электронного учебника.
4. Химические свойства углерода
Учитель: Рассмотрим химические свойства углерода.
Итак, исходя из электронного строения атома углерода, мы выяснили, что углерод может проявлять восстановительные и окислительные свойства. Причем при обычных условиях углерод химически малоактивен, однако при нагревании он реагирует со многими веществами. Таким образом, все реакции углерода протекают при высоких температурах (от 600-1700°С). Самой активной формой является аморфный углерод, менее активен графит, самый инертный – алмаз.
Учащиеся записывают уравнения химических реакций и проводят виртуальный лабораторный опыт «Горение угля в кислороде».
|
Углерод - восстановитель |
Углерод - окислитель |
|
При нагревании углерод соединяется с кислородом, образуя оксид углерода (IV), или углекислый газ: С + O2 = CO2 Виртуальный лабораторный опыт «Горение угля в кислороде».
При недостатке кислорода образуется оксид углерода (II), или угарный газ: 2С + О2 = 2СО |
С водородом углерод соединяется только при высоких температурах и в присутствии катализаторов. В зависимости от температуры образуются различные углеводороды, например, метан:
С + 2H2 |
|
Углерод взаимодействует при нагревании с серой и фтором: С + 2S = CS2 (сероуглерод)
С + 2F2 |
С металлами или их оксидами углерод образует карбиды: 4Al + 3C = Al4C3 CaO + 2C = CaC2 + СО |
|
При нагревании с водяным паром он вытесняет из воды водород: Н2O + С = СО + Н2 |
|
|
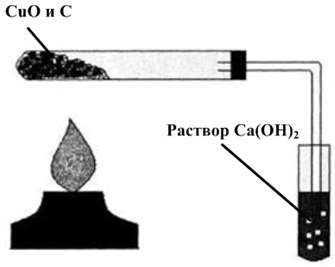
Углерод восстанавливает многие металлы из их оксидов: 2CuO + C = CO2 + 2Cu Демонстрационный опыт «Восстановление меди из оксида меди (II) углем»
|
|
Учитель проводит демонстрационный опыт «Восстановление меди из оксида меди (II) углем» (приложение 2).
5. Природные соединения углерода
Учитель: Итак, мы выяснили, что атомы углерода могут соединяться разнообразными способами между собой и с атомами многих других элементов, образуя огромное многообразие веществ. А в каком же виде углерод встречается в природе?
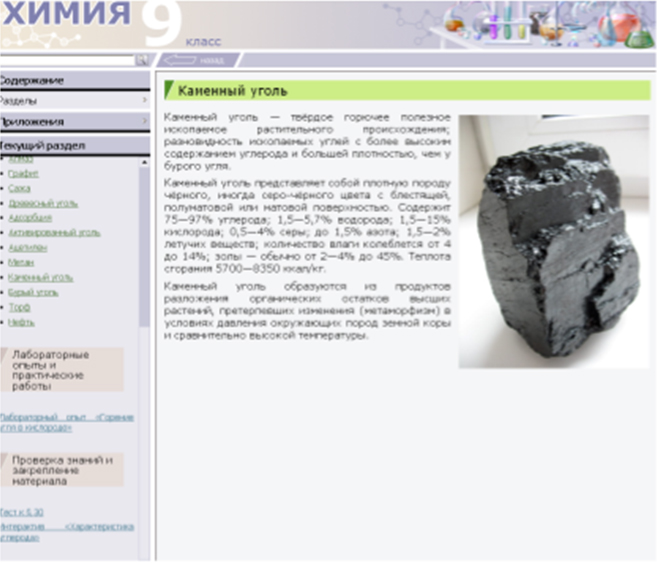
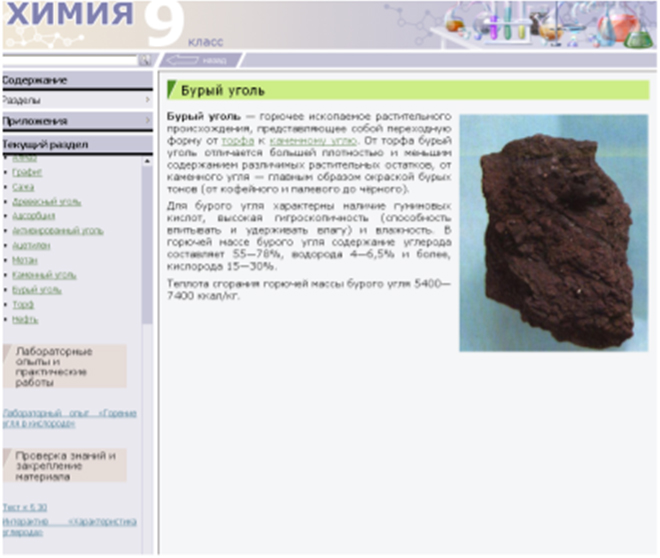
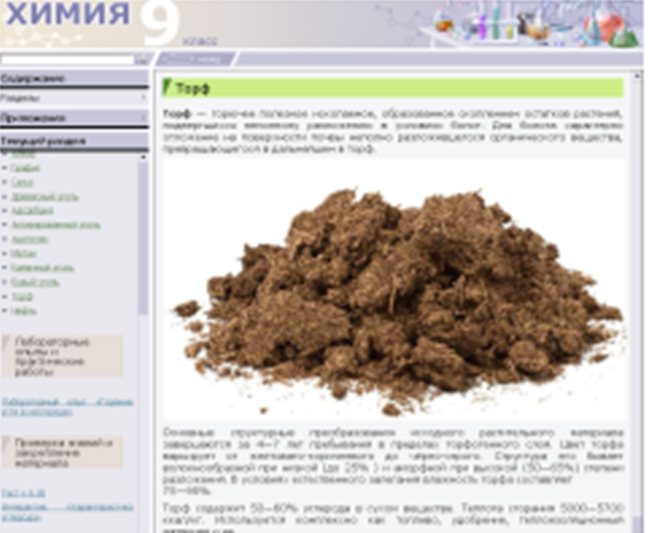
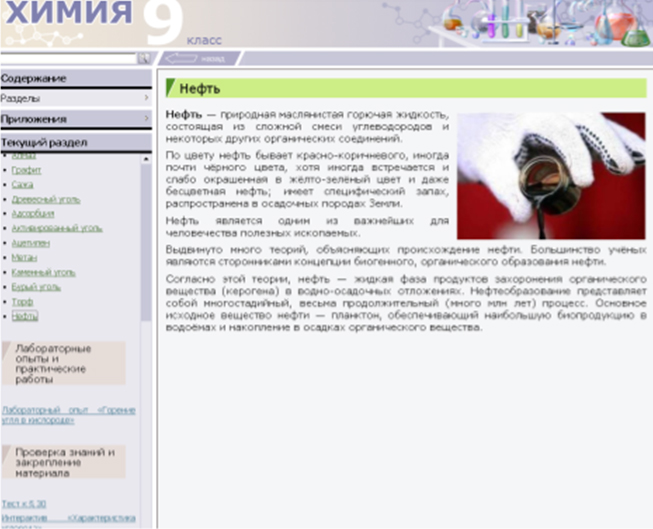
В природе углерод встречается как в свободном виде (алмаз, графит), так и в связанном. В связанном состоянии углерод входит в состав карбонатов (CaCO3 – мел, известняк, мрамор, MgCO3 – магнезит, CaCO3·MgCO3 – доломит), в каменных и бурых углях, торфе. Углерод входит в состав всех живых и растительных организмов, нефти, природного газа, углей.
Учащиеся знакомятся с природными соединениями углерода по дополнительному материалу из электронного учебника.
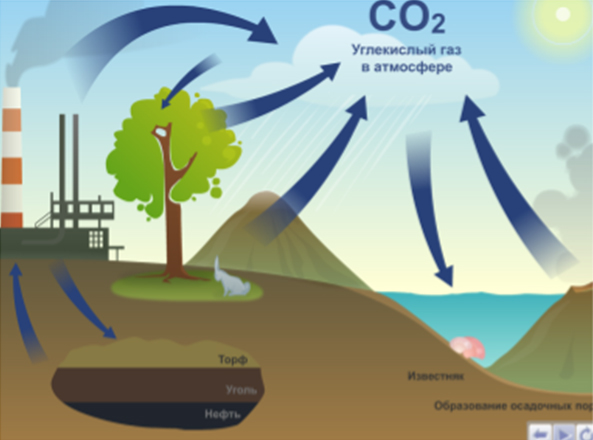
6. Круговорот углерода в природе
Учитель: все перечисленные источники углерода участвуют в круговороте его в природе. Учащиеся работают по материалу «Круговорот углерода в природе» электронного учебника (просмотр анимации).
IV. Этап первичного закрепления в обобщающей беседе
Учитель задает вопросы, учащиеся отвечают на них.
– Почему алмаз, графит и уголь называют «родными братьями»?
– От чего зависит твердость алмаза и мягкость графита?
– Для каких целей применяют алмаз и графит?
– О каком явлении рассказывается в сказке «Мороз Иванович»?
“Между тем Рукодельница воротится, воду процедит, в кувшины нальёт, да ещё какая затейница: коли вода нечиста, так свернет лист бумаги, наложит в неё угольков да песку крупного насыплет, вставит ту бумагу в кувшин да нальёт в неё воды, а вода-то знай проходит сквозь песок да сквозь уголья и капает в кувшин чистая, словно хрустальная”.
– Где еще в настоящее время широко используется явление адсорбции?
(Медицина, военное дело, химическая промышленность.)
– Назовите природные соединения углерода.
– Каковы химические свойства углерода?
– В каких условиях протекает большинство реакций с участием углерода?
– Чем объясняется не высокая химическая активность углерода?
– Какая из модификаций углерода химически наиболее активна?
V. Рефлексивно-оценочный этап (первичный контроль) – тестирование
Учитель предлагает проверить, как дети внимательно слушали друг друга и что запомнили.
Учащиеся работают в интерактиве «Характеристика углерода» электронного учебника.
После того, как они выполнили задания, на экран мультимедийного проектора отображаются критерии оценивания.
Учащиеся оценивают свою работу.
Рефлексия с помощью сигнальных карточек.
Учащиеся работают с сигнальными карточками, которые показывают итог тестирования.
Красные – рейтинг 5; синие – рейтинг 4; зеленые – рейтинг 3.
По желанию учащихся, полученные оценки можно выставить в журнал.
VI. Домашнее задание
Предлагается учащимся в двух формах:
1) обычной - по учебнику О.С. Габриеляна «Химия 9 класс» (М.: Дрофа, 2009) § 29, упр. 6,8;
2) творческой (по желанию):
• Выполнить творческое задание в программе «Power Point» по теме «Алмаз - уникальный камень» или написать сказку с участием углерода и прислать на электронный адрес учителя.
• Проделать дома опыт, доказывающий адсорбционные свойства угля.
Налейте в емкость воду объемом 40-50 см3 и добавьте 1-3 капли чернил, чтобы получился слабо окрашенный раствор. Затем добавьте 3-5 таблеток активированного угля и круговыми движениями колбы интенсивно перемешайте смесь. Дайте смеси отстоятся. Если обесцвечивания не произошло, добавьте еще 2-3 таблетки угля и повторите перемешивание. Убедившись, что адсорбция произошла полностью, профильтруйте смесь.
• Составить кроссворд по теме «Углерод»
• Подготовить краткое сообщение «Живопись глазами химика» по теме «Углерод. Графит. Сажа»
VII. Подведение итогов. Рефлексия
– Прочитайте цель урока. Достигли ли вы цели? В какой степени? Оцените свою работу на уроке.
Учитель подводит итог урока, проводит рефлексию, где учащиеся показывают результаты усвоения новых знаний, оценивают и комментируют работу наиболее активных учащихся.
Уходя с урока, учащиеся дорисовывают волосы заранее нарисованным рожицам: грустной или веселой в зависимости от их настроения и эмоционального состояния. По их шевелюре можно понять понравился ли урок или нет.
Список использованной литературы:
- Габриелян О.С. Химия. 9 класс: учебник для общеобразовательных учреждений - М.: Дрофа, 2012.
- Габриелян О.С. Настольная книга учителя. Химия. 9 класс», М.: Дрофа, 2002.
- Габриелян О.С. Химия 9 класс: рабочая тетрадь к учебнику Габриеляна О.С. «Химия.9» - М.: Дрофа, 2013.
- Габриелян О.С. Программа курса химии для 8-11 классов общеобразовательных учреждений- М.: Дрофа, 2012.
- Книга для чтения по неорганической химии. Ч.2/ Сост. В.А.Крицман – М:Просвещение, 1992
- Учебник – навигатор по химии 9 класс - М.: Дрофа,2013
- Химический эксперимент в школе/Т.С. Назарова, А.А. Грабецкий В.Н. Лаврова.- М.:Просвещение, 1987.
- Химия: Большой справочник для школьников и поступающих в вузы/Е.А.Алферова, Н.С.Ахметов, Н.В.Богомолова и др. - М.: Дрофа, 1999.




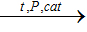 CH4
CH4
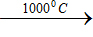 CF4 (фторид углерода)
CF4 (фторид углерода)