ЕГЭ-2018 по химии: разбор демоверсии задания 34
В этом материале представлен подробный разбор и алгоритмы решения 34 задания из демоверсии ЕГЭ-2018 по химии, а также даны рекомендации по использованию пособий для подготовки к ЕГЭ.Задание 34
При нагревании образца карбоната кальция часть вещества разложилась. При этом выделилось 4,48 л (н.у.) углекислого газа. Масса твердого остатка составила 41,2 г. Этот остаток добавили к 465,5 г раствора хлороводородной кислоты, взятой в избытке. Определите массовую долю соли в полученном растворе.
В ответе запишите уравнения реакций, которые указаны в условии задачи, и приведите все необходимые вычисления (указывайте единицы измерения искомых величин).

Ответ: Запишем краткое условие данной задачи.
Дано: V(CO2) = 4,48 л m() = 41,2 г. m(HCl) = 465,5 г |
Решение: Напишем уравнение первой реакции разложения карбоната кальция.
|
|||||||||||||||
Найти: ω% (СaCl2) |
После того как все приготовления приведены, приступаем к решению.
1) Определяем количество СО2, содержащееся в 4,48 л. его.
n(CO2) = V/Vm = 4,48 л / 22,4 л/моль = 0,2 моль
2) Определяем количество образовавшегося оксида кальция.
По уравнению реакции образуется 1 моль СО2 и 1 моль СаО
Следовательно: n(CO2) = n(CaO) и равняется 0,2 моль
3) Определяем массу 0,2 моль СаО
m(CaO) = n(CaO) · M(CaO) = 0,2 моль · 56 г/моль = 11,2 г
Таким образом, твердый остаток массой 41,2 г состоит из 11,2 г СаО и (41,2 г. – 11,2 г.) 30 г СаСО3
4)
Определим количество СаСО3, содержащееся в 30 г
n(CaCO3) = m(CaCO3) / M(CaCO3) = 30 г / 100 г/моль = 0,3 моль

Далее пишем следующие два уравнения необходимые для решения данной задачи:
CaO + HCl = CaCl2 + H2O
CaCO3 + HCl = CaCl2 + H2O + CO2
5) Определим количество хлорида кальция, образующееся в результате данных реакций.
В реакцию вступило 0,3 моль CaCO3 и 0,2 моль СаО всего 0,5 моль.
Соответственно, образуется 0,5 моль CaCl2
6) Рассчитаем массу 0,5 моль хлорида кальция
M(CaCl2) = n(CaCl2) · M(CaCl2) = 0,5 моль · 111 г/моль = 55,5 г.
7) Определяем массу углекислого газа. В реакции разложения участвовало 0,3 моль карбоната кальция, следовательно:
n(CaCO3) = n(CO2) = 0,3 моль,
отсюда:
m(CO2) = n(CO2) · M(CO2) = 0,3 моль · 44г/моль = 13,2 г.
8) Находим массу раствора. Она состоит из массы соляной кислоты + масс твердого остатка (CaCO3 + CaO) минут масса выделившегося CO2. Запишем это в виде формулы:
m(р-ра) = m(CaCO3 + CaO) + m(HCl) – m(CO2) = 465,5 г + 41,2 г – 13,2 г = 493,5 г.

9) И наконец, ответим на вопрос задачи. Найдем массовую долю в % соли в растворе, воспользовавшись следующим волшебным треугольником:
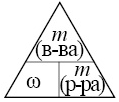
ω%(CaCI2) = m(CaCI2) / m(р-ра) = 55,5 г / 493,5 г = 0,112 или 11,2%
Ответ: ω % (СaCI2) = 11.2%