Задание 35 ЕГЭ по химии 2019
Представляем вашему вниманию разбор 35 задания ЕГЭ-2019 по химии.Блок «Химическая реакция. Методы познания в химии. Химия и жизнь. Расчеты по химическим формулам и уравнениям реакций»
Усвоение элементов содержания этого блока проверяется заданиями различного уровня сложности, в их числе 4 задания базового уровня сложности, 4 задания повышенного уровня сложности и 2 задания высокого уровня сложности.
Элементы содержания блока имеют прикладной и практико-ориентированный характер, что обусловливает некоторую особенность заданий, ориентированных на проверку усвоения данного материала.
Выполнение заданий этого блока предусматривает проверку сформированности следующих умений: использовать в конкретных ситуациях знания о применении изученных веществ и химических процессов, а также о промышленных методах получения некоторых веществ и способах их переработки; планировать проведение эксперимента по получению и распознаванию важнейших неорганических и органических веществ на основе приобретённых знаний о правилах безопасной работы с веществами в быту; проводить вычисления по химическим формулам и уравнениям.
Некоторые из элементов содержания данного блока, такие как определение характера среды водных растворов веществ, индикаторы, расчёты массовой или объёмной доли выхода продукта реакции от теоретически возможного, расчёты массовой доли (массы) химического соединения в смеси, проверялись в рамках одного задания в комплексе с другими элементами содержания.
Рассмотрим задания этого блока из демонстрационного варианта.
#ADVERTISING_INSERT#
В контрольной работе ЕГЭ по химии большая роль отведена расчетным задачам. Это объясняется тем, что при их решении необходимо опираться на знания химических свойств соединений, использовать умение составлять уравнения химических реакций, т.е. использовать во взаимосвязи теоретическую базу и определенные операционно-логические и вычислительные навыки.
Решение расчётных задач требует знания химических свойств веществ и предполагает осуществление некоторой совокупности действий, обеспечивающих получение правильного ответа. К таким действиям относятся:
- составление уравнений химических реакций (в соответствии с условием задачи), необходимых для выполнения стехиометрических расчетов;
- выполнение расчетов, необходимых для нахождения ответов на поставленные в условии задачи вопросы;
- формулирование логически обоснованного ответа на все поставленные в условии задания вопросы (например, определить физическую величину – массу, объём, массовую долю вещества).
Однако следует иметь в виду, что не все названные действия обязательно должны присутствовать при решении любой расчетной задачи, а в отдельных случаях некоторые из них могут использоваться неоднократно.
Согласно кодификатору элементов содержания и требований к уровню подготовки выпускников образовательных организаций, для проведения единого государственного экзамена по химии учащиеся должны уметь проводить следующие расчеты по химическим формулам и уравнениям реакций:
- расчеты с использованием понятия «массовая доля вещества в растворе»;
- расчеты объемных отношений газов при химических реакциях;
- расчеты массы вещества или объема газов по известному количеству вещества, массе или объему одного из участвующих в реакции веществ;
- расчеты теплового эффекта реакции;
- расчеты массы (объема, количества вещества) продуктов реакции, если одно из веществ дано в избытке (имеет примеси);
- расчеты массы (объема, количества вещества) продукта реакции, если одно из веществ дано в виде раствора с определенной массовой долей растворенного вещества;
- установление молекулярной и структурной формулы вещества;
- расчеты массовой или объемной доли выхода продукта реакции от теоретически возможного;
- расчеты массовой доли (массы) химического соединения в смеси.
При решении расчетных задач школьники часто допускают следующие типичные ошибки:
- не делают различия между массой раствора и массой растворенного вещества;
- при нахождении количества газообразного вещества делят его массу на молярный объем или, наоборот, делят объем газообразного вещества на его молярную массу;
- забывают расставить коэффициенты в уравнениях реакций;
- не находят, какое вещество в избытке (эта ошибка может быть связана также с отсутствием навыка решения задач на «избыток – недостаток»);
- при расчетах неправильно преобразовывают математические формулы, не задумываясь при этом об абсурдности полученного ответа (например, производят умножение, а не деление массы растворенного вещества на его массовую долю при нахождении массы раствора).
Большинство расчетных задач лучше решать в молях, так как этот способ является более рациональным. Однако сам способ решения и его рациональность при оценивании расчетных задач не учитываются. Главное, чтобы ученик продемонстрировал логику предложенного им способа решения и в соответствии с ним выполнил правильные вычисления, которые должны привести его к верному ответу.
Задачи высокого уровня сложности 34 и 35 не всегда доступны даже школьникам с хорошим и отличным уровнем подготовки. При решении задачи 35 многие школьники не понимают химизм процессов, описанных в задаче, и допускают ошибки при составлении уравнений реакций. Так, непонимание того, что означает фраза «часть вещества разложилась», не позволяет этим ученикам составить уравнения соответствующих реакций и провести по ним необходимые вычисления. Другая типичная ошибка связана с определением массы полученного раствора, что в итоге приводит к неверному нахождению искомой массовой доли веществ в растворе.
Задание 35
Органическое вещество А содержит 11,97% азота, 9,40% водорода и 27,35% кислорода по массе и образуется при взаимодействии органического вещества Б с пропанолом-2. Известно, что вещество Б имеет природное происхождение и способно взаимодействовать как с кислотами, так и со щелочами.
На основании данных условий задания:
- проведите необходимые вычисления (указывайте единицы измерения искомых физических величин) и установите молекулярную формулу исходного органического вещества;
- составьте структурную формулу этого вещества, которая однозначно отражает порядок связи атомов в его молекуле;
- напишите уравнение реакции получения вещества А из вещества Б и пропанола-2 (используйте структурные формулы органических веществ).
Вариант ответа:
Проведены вычисления и найдена молекулярная формула вещества А. Общая формула вещества А – CxHyOzNm.
w(C) = 100 – 9,40 – 27,35 – 11,97 = 51,28%
x : y : z : m = 51,28 / 12 : 9,4 / 1 : 27,35 / 16 : 11,97 / 14 = 5 : 11 : 2 : 1.
Молекулярная формула вещества А – C5H11O2N
Составлена структурная формула вещества А:
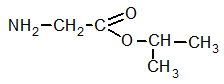
Написано уравнение реакции получения вещества А:
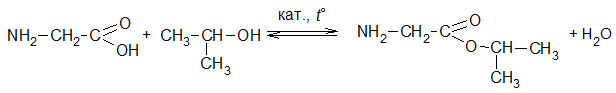
Трудности возникают у школьников при составлении структурной формулы искомого органического вещества, однозначно отражающей его свойства, а также при составлении уравнения реакции в соответствии с условием задачи. Лишь 25,7% участников экзамена смогли в 2018 г. полностью справиться с этой задачей и получить максимальные 3 балла за ее решение.
Необходимо отметить, задания с развёрнутым ответом могут быть выполнены выпускниками различными способами.
В заключение выделим несколько основных принципов организации подготовки школьников к экзамену.
Главной задачей подготовки к экзамену должна стать целенаправленная работа по повторению, систематизации и обобщению изученного материала, по приведению в систему знаний ключевых понятий курса химии.
Нельзя также сводить подготовку к экзамену только к тренировке в выполнении заданий, аналогичных заданиям экзаменационной работы текущего года. Следует широко использовать задания различных типов в различных форматах, которые нацелены не на простое воспроизведение полученных знаний, а на проверку сформированности умений применять теоретические знания в новых учебных ситуациях.
При изучении, повторении и закреплении учебного материала необходимо использовать различные задания, в том числе связанные с преобразованием информации из одной формы в другую: составлением обобщающих таблиц, граф-схем, диаграмм, графиков, конспектов и т.п.
И, конечно же, первостепенную роль при подготовке к экзамену играют опыт и знания, приобретенные школьниками при выполнении и обсуждении результатов реального химического эксперимента, которому следует уделить особое внимание в процессе изучения школьного курса химии.